2.25 ℃时CH3COONa 溶液的 Kw大于 100 ℃时NaOH 溶液的 Kw( )
3.NaCl 溶液和 CH3COONH4溶液均显中性,两溶液中水的电离程度相同( )
4.温度一定时,在纯水中通入少量 SO2,水的电离平衡不移动,Kw不变( )
5.室温下,0.1 mol·L-1的HCl 溶液与 0.1 mol·L-1的NaOH 溶液中水的电离程度相等( )
答案 1.× 2.× 3.× 4.× 5.√
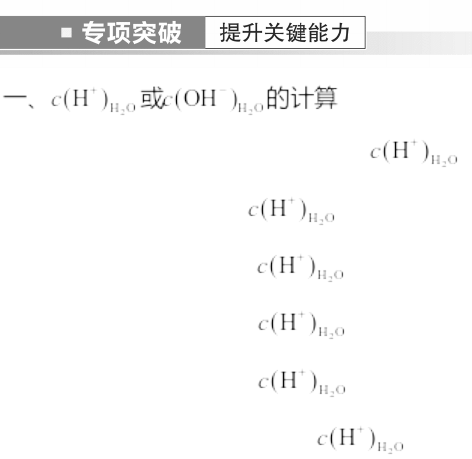
1.室温下,计算下列溶液中水电离出的 。
(1)0.01 mol·L-1的盐酸中, =___________________________________。
(2)pH=4的亚硫酸溶液中,
=___________________________________。
(3)pH=10 的KOH 溶液中, =___________________________________。
(4)pH=4的NH4Cl 溶液中, =__________________________________。
(5)pH=10 的CH3COONa 溶液中, =______________________________。
答案 (1)1×10-12 mol·L-1 (2)1×10-10 mol·L-1 (3)1×10-10 mol·L-1 (4)1×10-4 mol·L-1
(5)1×10-4 mol·L-1
2.常温时,纯水中由水电离出的 c(H+)=a mol·L-1,pH=1的盐酸中由水电离出的 c(H+)=
b mol·L-1,0.1 mol·L-1的盐酸与 0.1 mol·L-1的氨水等体积混合后,由水电离出的 c(H+)=
c mol·L-1,则 a、b、c的关系正确的是( )
A.a>b=c B.c>a>b C.c>b>a D.b>c>a
答案 B
解析 盐酸抑制水的电离,所以 b<a;0.1 mol·L-1的盐酸与 0.1 mol·L-1的氨水等体积混合后,
生成氯化铵溶液,铵根离子水解促进水的电离,则 c>a,故 B正确。
3.25 ℃时,在等体积的① pH=0的H2SO4溶液、② 0.05 mol·L-1的Ba(OH)2溶液、③ pH=
10 的Na2S溶液、④ pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是( )
A.1∶10∶1010∶109B.1∶5∶(5×109)∶(5×108)
C.1∶20∶1010∶109D.1∶10∶104∶109
答案 A
解析 H2SO4与Ba(OH)2抑制水的电离,Na2S与NH4NO3促进水的电离。25 ℃时,pH=0的
H2SO4溶液中:c(H2O)电离=c(OH-)= mol·L-1=10-14 mol·L-1;0.05 mol·L-1的Ba(OH)2溶液
中 : c(H2O) 电 离 =c(H +)= mol·L -1=10 -13 mol·L -1;pH =10 的Na2S溶 液 中 :