② 用漂白粉与浓盐酸制取少量氯气,化学方程式:__________________________________,
选用装置:______。
答案 Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O C
(4)铜与浓硝酸反应制取二氧化氮,选用装置:__________。
答案 C
(5)实验室制取乙烯的装置,可以通过选用上面哪个装置进行改进?若橡皮塞最多只允许打
两个孔,应如何改进所选实验装置:
________________________________________________________________________。
答案 D,将分液漏斗换成温度计(或将烧瓶换成蒸馏烧瓶,将导气管换成温度计)
(6)上述 B装置还能制取的气体有:______________________________________________。
答案 H2或H2S
2.气体的净化
(1)设计原则:根据主要气体及杂质气体的性质差异来选择除杂试剂及除杂装置。
(2)吸收剂的选择
选择吸收剂应根据被提纯气体的性质和杂质的性质来确定,一般情况如下:
① 易溶于水的气体杂质可用水来吸收;
② 酸性杂质可用碱性物质吸收;
③ 碱性杂质可用酸性物质吸收;
④ 水为杂质时,可用干燥剂来吸收;
⑤ 能与杂质发生反应生成沉淀(或可溶物)的物质也可作为吸收剂。
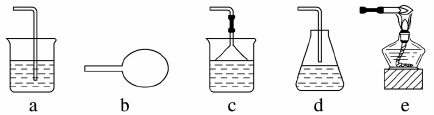
3.尾气处理装置的选择
a装置用于吸收或溶解反应速率不是很快的气体,如用 NaOH 溶液吸收 Cl2、CO2等。
b装置用于收集少量气体。
c、d装置用于吸收极易溶且溶解很快的气体,如 HCl、HBr、NH3等;其中 d装置吸收量较
少。
e装置用于处理难以吸收的可燃性气体,如 H2、CO 等。
4.实验条件的控制
(1)排气方法
为了防止空气中的 O2、CO2、水蒸气等干扰实验,常用其他稳定的气体(如氮气)排尽装置中
的空气;有时也可充分利用反应产物气体(如氨气、氯气、二氧化硫)等排尽装置中的空气。
(2)控制气体的流速及用量
① 用分液漏斗控制液体滴加的速度和用量。
② 观察气泡,控制气流速度,如图甲,可观察气泡得到 N2、H2的体积比约为 1∶3的混合气