第1章 第4讲 氧化还原反应---2023年高考化学一轮复习(新高考)
第4讲 氧化还原反应
复习目标 1.了解氧化还原反应的概念。2.会用“单、双线桥”分析电子转移的方向和数目。
3.掌握氧化性、还原性强弱的比较及价态规律应用。
考点一 氧化还原反应及相关概念
1.氧化还原反应
(1)判断依据:反应前后有元素的化合价发生变化。
(2)本质:电子转移(得失或偏移)。
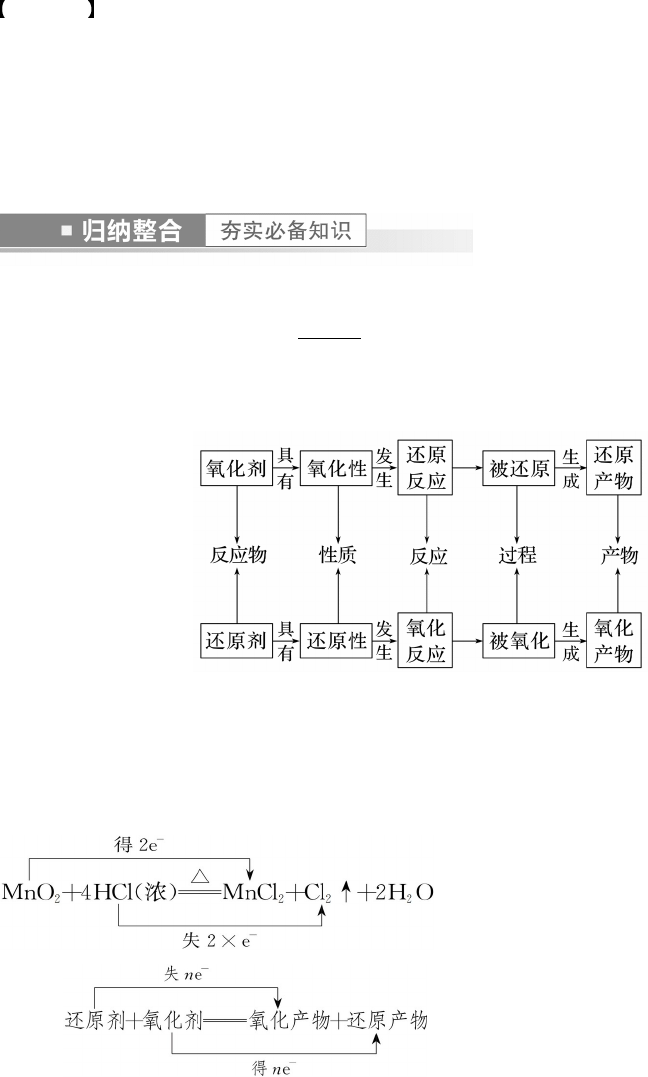
2.相关概念
概括为“升失氧、降得还,剂性一致、其他相反”。
3.氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价 ②画箭头(反应物指向生成物) ③算数目 ④说变化。
用双线桥法标出 MnO2与浓盐酸加热反应电子转移的方向和数目:
。
归纳 。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标
“得”“失”字样。
用单线桥法标出铜和浓硝酸反应电子转移的方向和数目:
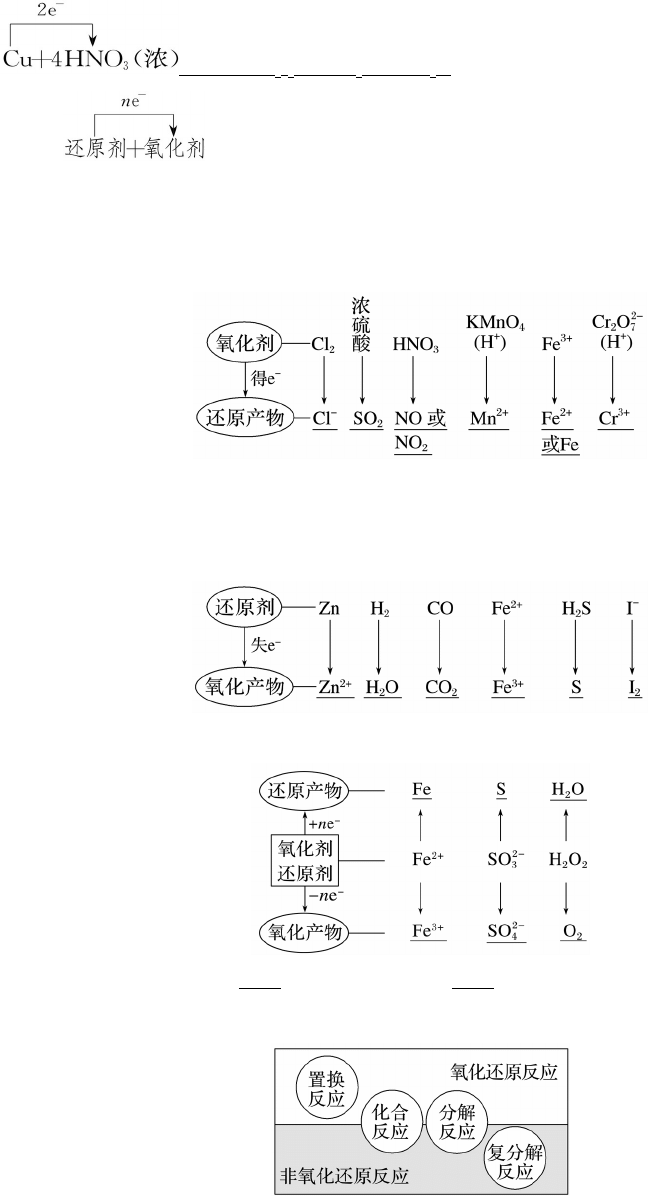
== =Cu(NO 3)2+ 2NO 2↑ + 2H 2O。
归纳 ===氧化产物+还原产物。
4.常见的氧化剂和还原剂
(1)常见的氧化剂
常见的氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
(2)常见的还原剂
常见的还原剂包括活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离
子、某些非金属单质及其氢化物等。如:
(3)元素化合价处于中间价态的物质既有氧化性,又有还原性。如:
其中:Fe2+、SO 主要表现还原性,H2O2主要表现氧化性。
5.氧化还原反应与四种基本反应类型间的关系图示
6.重要的还原剂——金属氢化物、NaBH4
(1)金属氢化物
① 结构特点
电子式可表示为 M+[H]-(M 为碱金属)。
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币





