(6)改变外界条件对多平衡体系的影响。
一、投料比、转化率相关图像
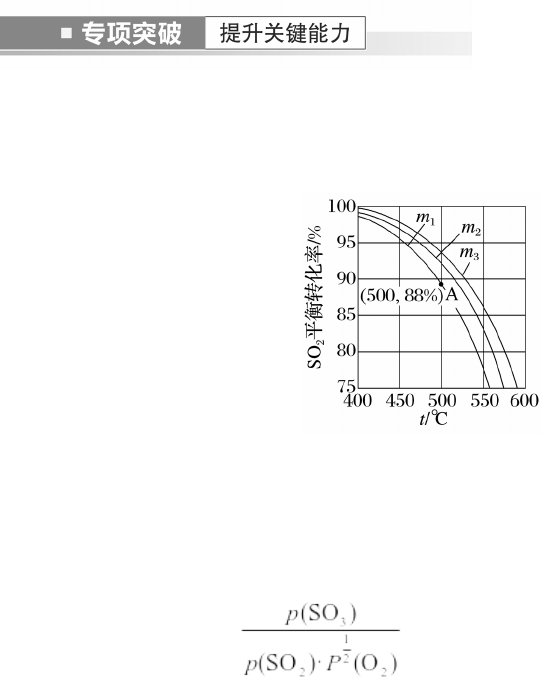
1.在保持体系总压为 105 Pa 的条件下进行反应:SO2+O2SO3,原料气中 SO2和O2的物质
的量之比 m[m=]不同时,SO2的平衡转化率与温度(t)的关系如图所示:
(1)图中 m1、m2、m3的大小顺序为________。反应的化学平衡常数 Kp表达式为________(用
平衡分压代替平衡浓度表示)。
(2)图中 A点原料气的成分:n(SO2)=10 mol,n(O2)=24.4 mol,n(N2)=70 mol,达平衡时
SO2的分压 p(SO2)为________ Pa(分压=总压×物质的量分数)。
答案 (1)m1>m2>m3 Kp=
(2)1 200
解析 (1)在同温同压下,增加二氧化硫的量,会使原料气中 SO2和O2的物质的量之比 m变
大,m越大,平衡转化率 α(SO2)越小。
(2)A 点二氧化硫的平衡转化率为 88%,可进行如下计算:
SO2(g) + O2(g) SO3(g)
起始/mol 10 24.4 0
变化/mol 10×88% ×10×88% 10×88%
平衡/mol 10×12% 24.4-5×88% 10×88%
平衡时,混合气体总量为 10×12%+(24.4-5×88%)+10×88%+70=100 mol。达平衡时
SO2的分压 p(SO2)=×105=1 200 Pa。
2.采用一种新型的催化剂(主要成分是 Cu—Mn 合金),利用 CO 和H2制备二甲醚(DME)。
主反应:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)
副反应:CO(g)+H2O(g)CO2(g)+H2(g)
CO(g)+2H2(g)CH3OH(g)
测得反应体系中各物质的产率或转化率与催化剂的关系如图所示。