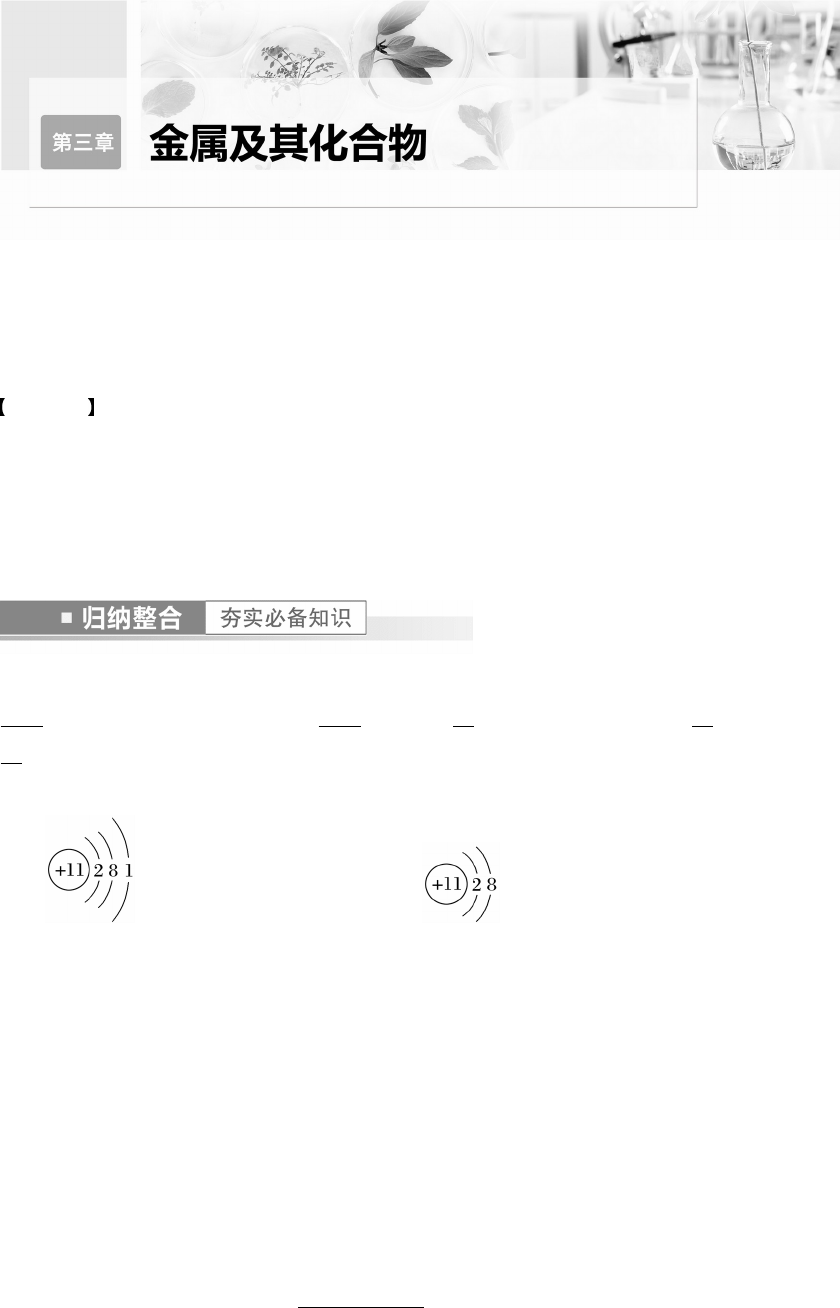
(1)钠钾合金(液态)可用于原子反应堆的导热剂。
(2)用作电光源,制作高压钠灯。
(3)冶炼某些金属
金属钠具有强还原性,熔融状态下可以用于制取金属,如 4Na+TiCl4=====4NaCl+Ti。
1.钠可以保存在四氯化碳溶液中( )
2.金属钠着火时,可用泡沫灭火器或干燥的沙土灭火( )
3.钠表面自然形成的氧化层能够保护内层金属不被空气氧化( )
4.金属钠具有强还原性,可与 TiCl4溶液反应制取金属 Ti( )
5.钠的金属性比钾强,工业上用钠制钾的原理为 Na+KClK↑+NaCl( )
6.实验结束后剩余的金属钠不能随意丢弃,应放回原试剂瓶中( )
答案 1.× 2.× 3.× 4.× 5.× 6.√
一、钠与水反应的信息提取
1.用镊子从煤油中取出一块钠,用滤纸吸干表面的煤油后,用小刀切取两小块钠,截面呈
银白色,很快变暗。
将其中一小块钠投入盛有水的烧杯中,盖上玻璃片。发现钠浮于水面并四处游动,滴有酚酞
的水变为红色。
将另一小块钠投入盛有水和苯各 10 mL 试管中。观察到钠在苯和水的界面处反应并上下跳
动。
上述实验你能提取哪些有关钠的相关信息(试从性质、保存等方面回答)?
答案 (1)保存:Na 应保存在煤油中。
(2)钠为银白色固体,质地较软(硬度小),密度比水小,比煤油、苯大。
(3)易被 O2氧化,与水剧烈反应,生成碱。
二、钠与溶液反应的分析方法
2.钠与水溶液反应的本质是与水电离的氢离子反应,思考解答下列问题:
将一小块金属钠分别投入盛有:a.水、b.乙醇、c.稀H2SO4的三个小烧杯中,反应速率由大
到小的顺序为________。解释反应速率不同的原因:__________________________________。
答案 c>a>b 钠与上述三种物质反应的实质都是钠与 H+之间的置换反应,由三种物质电
离出 H+的能力可知反应速率的大小顺序为 c>a>b
3.将一小块钠投入硫酸铜溶液中,剧烈反应,生成蓝色沉淀(仔细观察,发现还有少量黑色
沉淀)。
(1)写出钠与硫酸铜溶液反应的离子方程式。
(2)黑色沉淀的成分是什么?