C.加热 Fe(OH)3发生转化⑥,加水溶解可实现转化③
D.由图可预测:高铁酸盐 (FeO)具有强氧化性,可用于消毒, FeO 与水反应最终可生成
Fe(OH)3胶体,从而吸附水中的悬浮物,故高铁酸盐可作净水剂
答案 D
解析 铁与高温水蒸气反应生成四氧化三铁和氢气,不能实现上述转化①,故 A错误;FeO
是一种黑色粉末,不稳定,在空气中受热,部分被氧化生成 Fe3O4,不能发生转化②,故 B
错误;加热 Fe(OH)3发生转化⑥分解生成氧化铁,氢氧化铁不溶于水,加水溶解不可实现转
化③,故 C错误;高铁酸盐中铁为+6价,具有强氧化性,可用于消毒,与水发生氧化还原
反应后生成铁离子,铁离子与水反应生成 Fe(OH)3胶体。
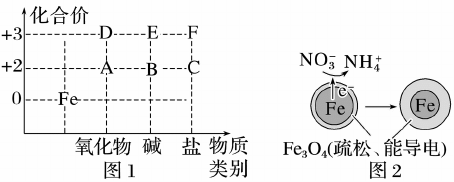
2.从化合价和物质类别两个视角认识元素及其化合物性质是重要的化学学习方式。图 1是
Fe 及其化合物的化合价—物质类别二维图。
回答下列问题:
(1)工业上冶炼 Fe 常用的方法是__________________________________________
(填字母)。
a.电解法 b.还原法 c.热分解法 d.物理方法
(2)若图 1中的 F为硫酸盐,请写出由 D生成 F的离子方程式:___________________。
(3)图1中的 B在潮湿的空气中很容易发生化合反应变成 E,该反应的化学方程式为
_________________________________________________________________________。
(4)图1中的 F与C在水溶液中转化的离子反应有:2Fe3++2I-2Fe2++I2,为了探究该反
应存在一定的限度,某化学兴趣小组取 10 mL 0.5 mol·L-1的KI 溶液于试管中,再加入 10
mL 0.2 mol·L-1的FeCl3溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目
的,还需要再向试管中加入下列试剂中的________(填字母)。
A.淀粉溶液 B.KSCN 溶液 C.CCl4 D.酸性高锰酸钾溶液
(5)用Fe 可以去除水体中的 NO(原理如图 2)。若有 1 mol NO 转化为 NH,则参加反应的 Fe
失去的电子的物质的量为________mol。
答案 (1)b (2)Fe2O3+6H+===2Fe3++3H2O
(3)4Fe(OH)2+O2+2H2O===4Fe(OH)3
(4)B (5)8
解析 (1)工业上常用碳还原铁矿石冶炼 Fe,为还原法。(2)根据图 1,D到F过程中铁的化
合价未变,F为硫酸盐,则 D为氧化铁,氧化铁与硫酸反应生成硫酸铁和水,离子方程式为