第3章 第15讲 金属材料 金属冶炼---2023年高考化学一轮复习(新高考)
第15 讲 金属材料 金属冶炼
复习目标 1.了解镁、铝、铜单质及其重要化合物的性质、用途和制备方法。2.了解常见金
属的活动性顺序。3.了解合金的概念及金属材料的重要应用。
考点一 铝及其化合物
(一)铝的结构与性质
1.铝的结构和存在
铝位于元素周期表的第三周期第Ⅲ
族,原子结构示意图: ,是活泼金属,在自然
界中以化合态的形式存在,铝是地壳中含量最多的金属元素。
2.铝的物理性质
银白色有金属光泽的固体,有良好的延展性、导电性和导热性等,密度、硬度均较小。
3.铝的化学性质
(1)与非金属单质的反应
① 与空气中的氧气形成致密的氧化膜。
② 与氯气加热反应的化学方程式:2Al+3Cl2=====2AlCl3。
(2)与水的反应
金属铝与水反应很困难。
(3)与酸的反应
①与H+反应的离子方程式:2Al+6H+===2Al3++3H2↑。
② 在冷的浓硫酸、浓硝酸中钝化。
(4)与碱的反应
写出 Al 与NaOH 溶液反应的离子方程式:2Al+2OH-+2H2O===2AlO+3H2↑。
(5)与某些金属氧化物的反应
① 写出铝与 Fe2O3反应的化学方程式:2Al+Fe2O3=====2Fe+Al2O3。该反应称作铝热反应,
反应时放出大量的热。
② 铝热反应实验中的有关问题
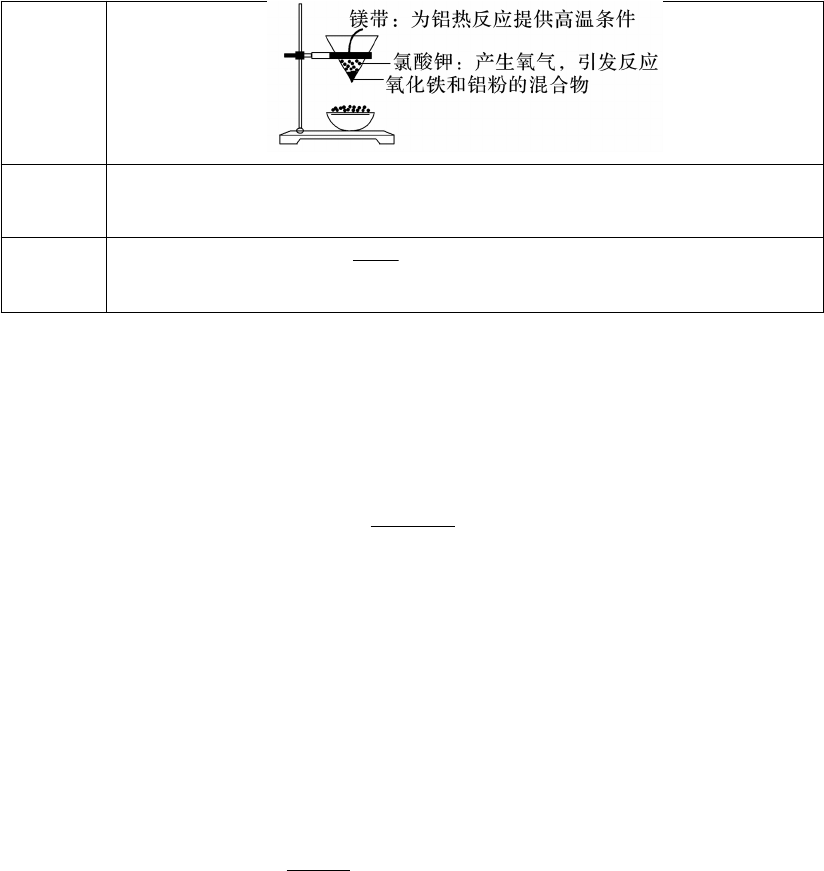
实验
装置
实验
现象
① 镁带剧烈燃烧,放出大量的热,并发出耀眼的白光,氧化铁与铝粉在较
高温度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中
原理
应用
① 制取熔点较高、活动性弱于
Al 的金属,如铁、铬、锰、钨等;
② 金属焊接,如野外焊接钢轨等
(6)铝的冶炼
2Al2O3(熔融)=======4Al+3O2↑。
(二)Al2O3的性质
1.物理性质
白色粉末,不溶于水,熔点高,是优良的耐火材料。
2.化学性质
(1)与H2O不反应。
(2)两性氧化物
分别写出 Al2O3与盐酸、NaOH 溶液反应的离子方程式:
① 与盐酸反应:Al2O3+6H+===2Al3++3H2O。
②与NaOH 溶液反应:Al2O3+2OH-===2AlO+H2O。
(三)Al(OH)3的性质
1.物理性质
不溶于水的白色胶状固体,具有吸附性。
2.不稳定性
加热时,氢氧化铝易分解,反应的化学方程式:2Al(OH)3=====Al2O3+3H2O。
3.两性——溶于强酸、强碱
分别写出 Al(OH)3与稀硫酸、NaOH 溶液反应的离子方程式。
(1)与稀硫酸反应
Al(OH)3+3H+===Al3++3H2O。
(2)与NaOH 溶液反应
Al(OH)3+OH-===AlO+2H2O。
4.Al(OH)3的制备
写出下列反应的离子方程式
(1)Al3+与氨水反应(不用强碱)
Al3++3NH3·H2O===Al(OH)3↓+3NH。
(2)AlO 溶液中通入过量的 CO2
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币

