第4章 第18讲 氯及其化合物---2023年高考化学一轮复习(新高考)

第18 讲 氯及其化合物
复习目标 1.了解氯的单质及其重要化合物的制备方法,掌握其主要性质及应用。2.了解氯
的单质及其重要化合物对环境的影响。
考点一 氯及其化合物的性质和应用
(一)氯气的性质
1.氯气的物理性质
氯气是一种黄绿色,有刺激性气味的气体,密度比空气的大,沸点-34.6 ℃,易液化。
注意 实验室里闻有毒气体及未知气体气味的方法是:用手在瓶口轻轻扇动,仅使极少量气
体飘进鼻孔(如图所示)。
2.氯的原子结构示意图: 。
3.氯气的化学性质
(1)氧化性
(2)从化合价的角度认识 Cl2的化学性质——歧化反应
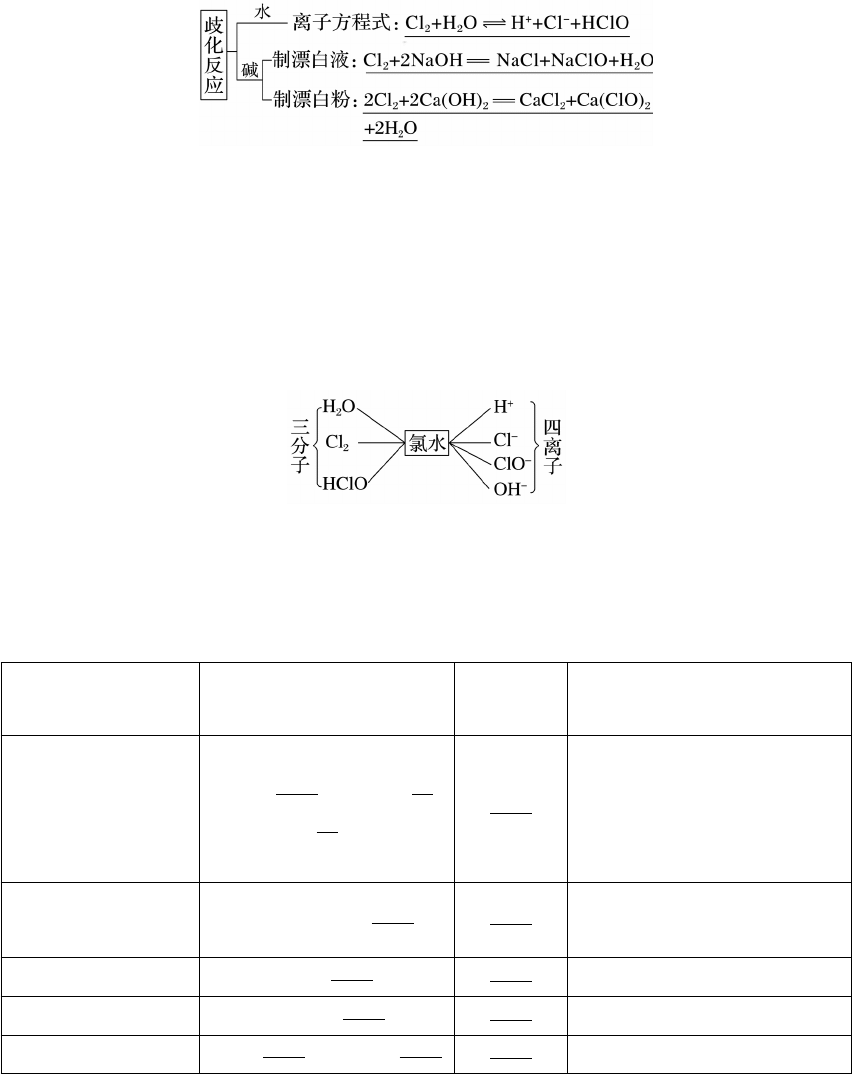
氯气与水或碱反应,氯元素的化合价既有升高又有降低,因而氯气既表现氧化性又表现还原
性。
4.从平衡的角度理解氯水的成分和性质
氯气能以 1∶2的比例溶于水中,氯气的水溶液称为氯水,溶于水的氯气只有少量与水反应。
(1)氯水中存在三种平衡关系:
①Cl2+H2OHCl+HClO
②HClOH++ClO-
③H2OH++OH-
(2)氯水性质的多重性
新制氯水的多种成分决定了它具有多重性质,在不同的化学反应中,氯水中参与反应的微粒
不同。
完成下列表格:
向氯水中加入的物
质或改变的条件 浓度变化 平衡移动
的方向 应用
可溶性氯化物
c(Cl-)增大,c(HClO)减
小左移
① 用饱和食盐水除 Cl2中的
HCl
② 用排饱和食盐水法收集
Cl2
盐酸 c(H+)和c(Cl-)增大 左移 洁厕剂和“84”消毒液不宜
混合使用
NaOH c(H+)减小 右移 用NaOH 吸收多余的 Cl2
光照 c(HClO)减小 右移 氯水应避光保存或现用现配
碳酸钙 c(H+)减小,c(HClO)增大 右移 制取次氯酸浓度较大的氯水
注 氯水常代替氯气进行溶液中的实验。
(二)次氯酸和次氯酸盐的性质
1.次氯酸
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币





