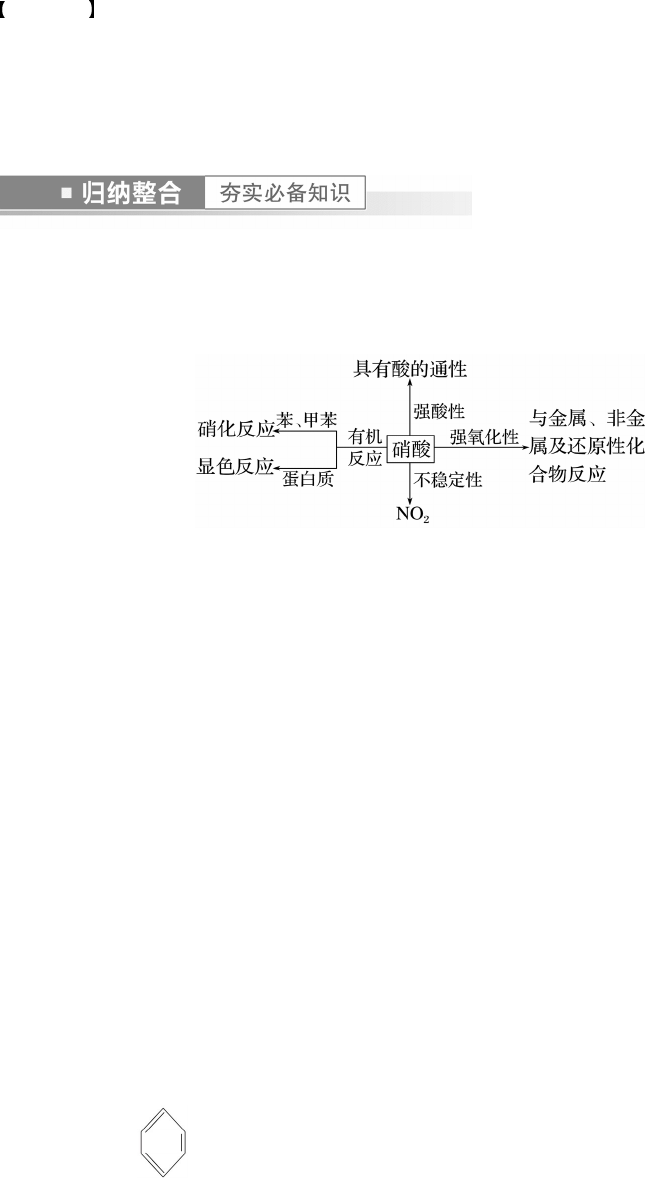
+HNO3――→ +H2O;
② 显色反应:含有苯基的蛋白质遇到浓硝酸时变黄色。
1.常温下,铁、铝在浓硝酸中的钝化为化学变化( )
2.可用稀 HNO3与FeS 固体反应制取 H2S( )
3.铜、碳分别与浓 HNO3反应,都体现了浓硝酸的强氧化性和酸性( )
4.在酸性条件下,NO 与I-、Fe2+、SO 等离子均不能大量共存( )
5.Cu 在KNO3溶液和稀 H2SO4中均不溶解,但能溶解在其混合液中( )
6.试管内壁上的银镜可用稀 HNO3除去,也可用氨水除去( )
7.浓 HNO3和氯水均用棕色试剂瓶保存,其原理相同( )
8.浓 HNO3溅到皮肤上,皮肤会变黄( )
答案 1.√ 2.× 3.× 4.√ 5.√ 6.× 7.√ 8.√
一、金属与硝酸反应的定性分析
1.用动态观点理解 Cu 与浓 HNO3的反应
向一定量的浓硝酸中加入过量的铜片。
(1)反应开始阶段产生________________色气体,化学方程式为_________________。
(2)反应进行一段时间后又产生无色气体,此时的化学方程式为_________________。
(3)待反应停止后,再加入少量的稀硫酸,这时 Cu 片上又有气泡产生,原因是____________
___________________________________________________________________
______________________________________________________________________________。
答案 (1) 红棕 Cu +4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O (2)3Cu +8HNO3(稀)=
==3Cu(NO3)2+2NO↑+4H2O (3)加入稀硫酸后,氢离子与原溶液中的硝酸根离子构成强氧
化性酸,又能与过量的铜反应
二、金属与硝酸反应的定量计算
2.在 100 mL 稀HNO3和稀 H2SO4组成的混合溶液中,两种酸的物质的量浓度之和为 0.4
mol·
L-1。向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中 Cu2+的物质的量浓度最
大值为________________(反应前后溶液体积变化忽略不计)。
答案 0.24 mol·L-1
解析 反应的离子方程式为 3Cu+2NO+8H+===3Cu2++2NO↑+4H2O,铜足量,由上述反
应方程式可知,NO 和H+的物质的量之比为 1∶4时,反应生成的铜离子物质的量最大,设