热点强化 7 臭氧和过氧化氢
1.臭氧
(1)组成:臭氧的分子式为 O3,与 O2互为同素异形体。
(2)物理性质:常温常压下,臭氧是一种有特殊臭味的淡蓝色气体,密度比氧气大,比氧气
易溶于水。吸入少量臭氧对人体无害,吸入过量臭氧对人体健康有一定危害。
(3)化学性质
不稳定性 O3不稳定,容易分解,反应的化学方程式为 2O3===3O2,在放电条件下
空气中的 O2可以转化为 O3,反应的化学方程式为 3O2=====2O3
强氧化性 O3容易使淀粉-KI 溶液变蓝色,反应的化学方程式为 2KI+O3+
H2O===I2+2KOH+O2
漂白性 O3因其强氧化性能使有色物质褪色
(4)用途
① 可用作脱色剂和消毒剂;
② 臭氧层可以吸收来自太阳的紫外线,是人类和其他生物的保护伞。
2.过氧化氢
(1)结构
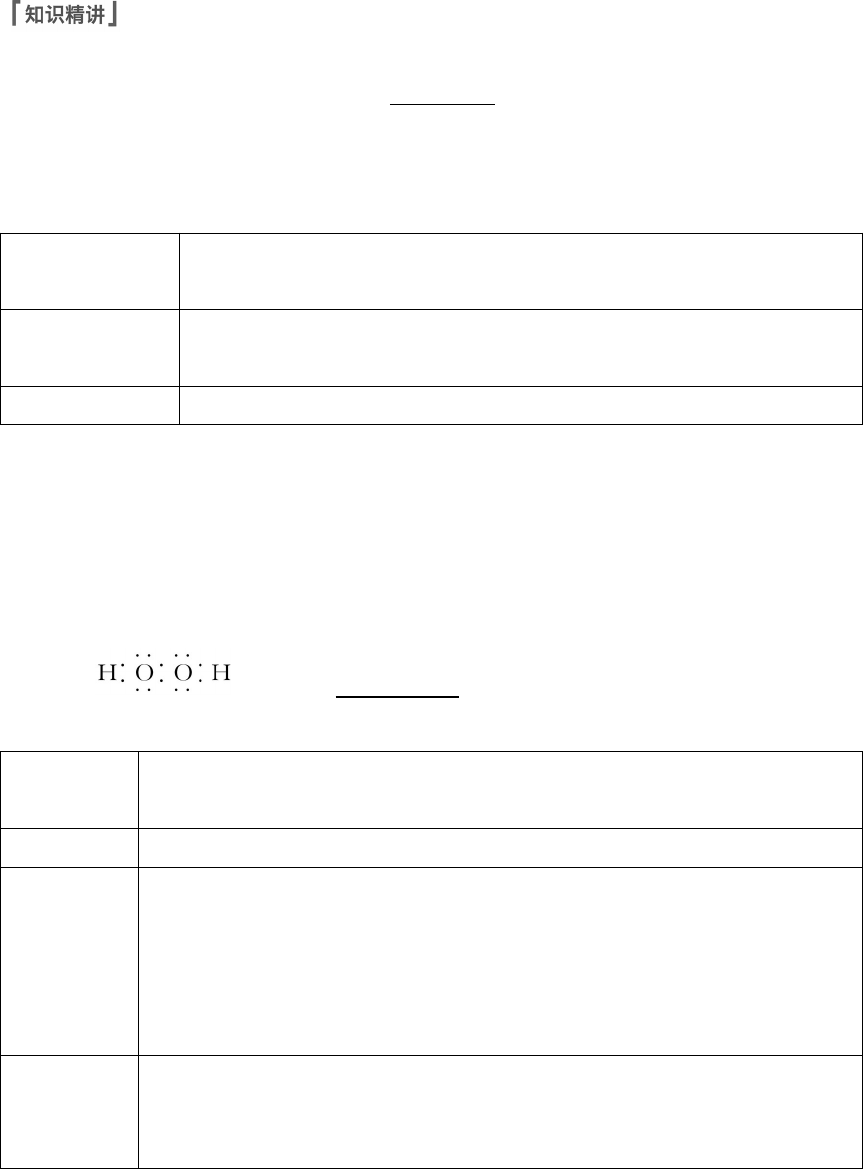
电子式: ,结构式:H—O—O—H。
(2)化学性质
不稳定性 加热、光照或加催化剂都能加快其分解:2H2O2=====2H2O+O2↑,因此
H2O2应保存在棕色瓶中并放置在阴凉处
弱酸性 相当于二元弱酸:H2O2H++HO,HOH++O
强氧化性
① 工业上用 10%的H2O2作为漂白剂,医疗上用 3%的H2O2作为消毒杀菌
剂;
②氧化Fe2+、SO 等还原性物质:H2O2+2Fe2++2H+===2Fe3++2H2O,H2O2
+Na2SO3===Na2SO4+H2O;
③ 使湿润的淀粉-KI 试纸变蓝:H2O2+2I-+2H+===I2+2H2O
弱还原性
H2O2中-1价的氧遇强氧化剂可失去电子转化成 0价氧而被氧化,如与酸性
KMnO4溶液反应:2KMnO4+5H2O2+3H2SO4===K2SO4+2MnSO4+5O2↑+
8H2O