第5章 第26讲 原子结构 核外电子排布原理---2023年高考化学一轮复习(新高考)

第26 讲 原子结构 核外电子排布原理
复习目标 1.了解元素、核素和同位素的含义。2.了解原子的构成,了解原子序数、核电
荷数、质子数、中子数、核外电子数以及它们之间的关系。3.了解原子核外电子的运动状态、
能级分布和排布原理,能正确书写 1~36 号元素原子核外电子、价电子的排布式和轨道表示
式。4.了解电子在原子轨道之间的跃迁及其简单应用。
考点一 原子结构 核素 同位素
1.原子构成
(1)构成微粒及作用
(2)微粒间的数量关系
① 阳离子的核外电子数=质子数-所带电荷数。
② 阴离子的核外电子数=质子数+所带电荷数。
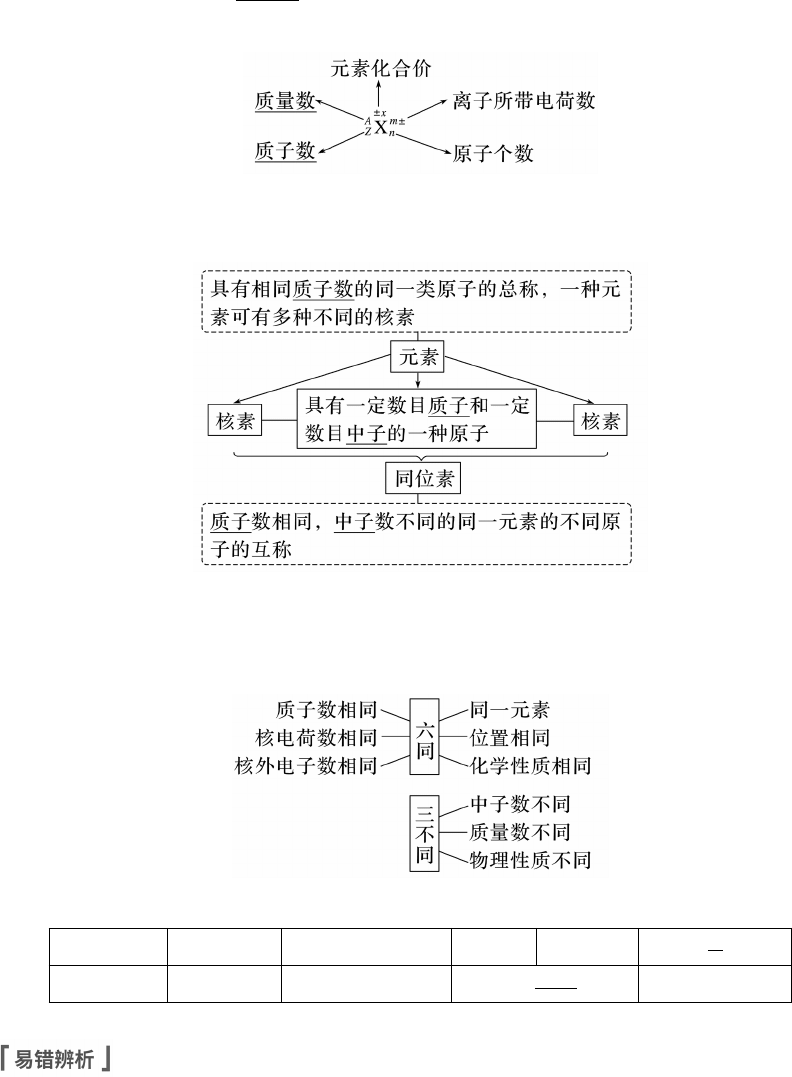
(3)微粒符号周围数字代表的信息
2.元素、核素、同位素
(1)元素、核素、同位素的概念及关系
(2)同位素
① 天然存在同一元素的各核素所占原子百分数一般不变。
② 同位素的“六同”与“三不同”
(3)常见的重要核素及其应用
核素 UCH H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
1.中子数为 10 的氧原子:O( )
2.核聚变如 H+H―→He+n,因为有新微粒生成,所以该变化是化学变化( )
3.Cl 与Cl 得电子能力几乎相同( )
4.一种元素只有一种核素,有多少种核素就有多少种原子( )
5.所有的原子中都含有质子和中子,任何离子都有电子( )
6.质量数就是元素的相对原子质量( )
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币





