第5章 第27讲 元素周期表和元素周期律---2023年高考化学一轮复习(新高考)
第27 讲 元素周期表和元素周期律
复习目标 1.能从原子价层电子数目和价层电子排布的角度解释元素周期表的分区、周期
和族的划分,能列举元素周期律(表)的应用。2.了解元素电离能、电负性的含义,能描述主
族元素第一电离能、电负性变化的一般规律,能从电子排布的角度对这一规律进行解释,能
说明元素电负性大小与原子在化合物中吸引电子能力的关系,能利用电负性判断元素的金属
性与非金属性的强弱、推断化学键的极性。
考点一 元素周期表的结构
1.元素周期表的编排原则
2.元素周期表的结构
(1)周期(7 个横行,7个周期)
短周期 长周期
周期序数 一 二 三 四 五 六 七
元素种数 2 8 8 18 18 32 32
(2)族(18 个纵列,16 个族)
主族 列1 2 13 14 15 16 17
族ⅠAⅡAⅢAⅣAⅤAⅥAⅦA
副族 列 3 4 5 6 7 11 12
族ⅢBⅣBⅤBⅥBⅦBⅠBⅡB
Ⅷ族 第8 、 9 、 10
纵列
3.原子结构与元素周期表的关系
(1)原子结构与周期的关系
原子的最大能层数=周期序数
(2)原子结构与族的关系
① 主族元素的价层电子排布特点
主族 ⅠAⅡAⅢAⅣA
排布特点 n s 1
n s 2
n s 2
n p 1
n s 2
n p 2
主族 ⅤAⅥAⅦA
排布特点 n s 2
n p 3
n s 2
n p 4
n s 2
n p 5
②0族元素的价层电子排布:He 为1s2;其他为 ns2np6。
③ 过渡元素(副族和第Ⅷ族)的价层电子排布:(n-1)d1~10ns1~2。
4.元素周期表中的特殊位置
(1)按元素种类
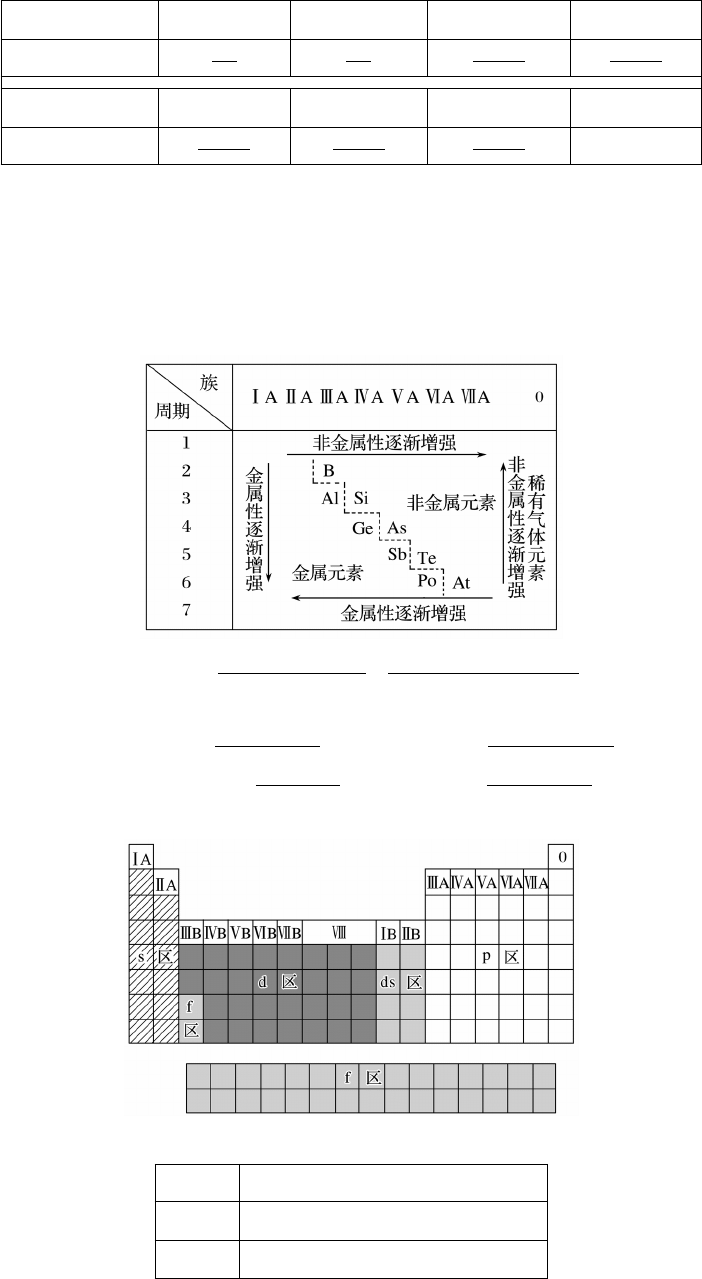
a.分界线:沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条虚线,
即为金属元素区和非金属元素区的分界线。
b.各区位置:分界线左下方为金属元素区,分界线右上方为非金属元素区。
c.分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
(2)按价层电子排布
各区价层电子排布特点
分区 价层电子排布
s区ns1~2
p区ns2np1~6(除He 外)
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币





