第5章 第29讲 化学键 分子的空间结构---2023年高考化学一轮复习(新高考)
第29 讲 化学键 分子的空间结构
复习目标 1.了解化学键的定义,了解离子键、共价键的形成。2.了解共价键的类型、共价
键的参数及作用。3.掌握电子式的书写。4.了解价层电子对互斥模型和杂化轨道理论的内容
并能用其推测简单分子或离子的空间结构。
考点一 化学键 电子式
1.化学键
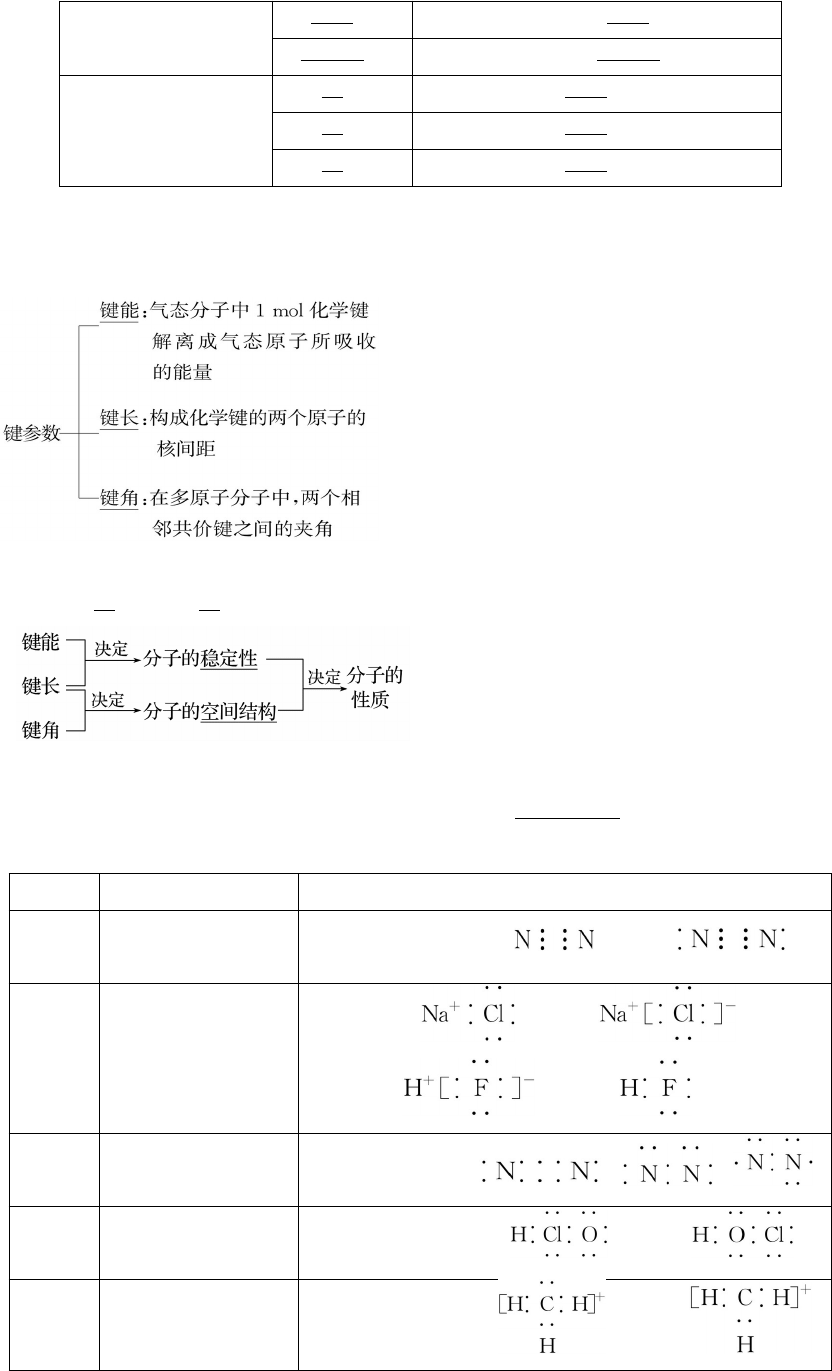
(1)化学键的定义及分类
(2)离子键、共价键的比较
离子键 共价键
成键粒子 阴、阳离子 原子
成键实质 阴、阳离子的静电作用 共用电子对与成键原子间的静电作用
形成条件
活泼金属与活泼非金属经电子得
失,形成离子键;铵根离子与酸根
离子之间形成离子键
同种元素原子之间成
键
不同种元素原子
之间成键
形成的
物质 离子化合物
非金属单质(稀有气
体除外);某些共价
化合物或离子化合物
共价化合物或某
些离子化合物
2.共价键
(1)特征
具有饱和性和方向性。
(2)分类
分类依据 类型
形成共价键的原子轨
道重叠方式
σ
形成共价键的电子对
是否偏移
极性键 共用电子对发生偏移
非极性键 共用电子对不发生偏移
原子间共用电子对的
数目
单键 原子间有一对共用电子对
双键 原子间有两对共用电子对
三键 原子间有三对共用电子对
(3)键参数
① 概念
② 键参数对分子性质的影响
a.键能越大,键长越短,分子越稳定。
b.
3.化学键的表示方法——电子式
(1)概念:在元素符号周围用“·”或“×”来表示原子的最外层电子的式子。
(2)电子式书写常见的 6大误区
内容 实例
误区 1
漏写未参与成键的
电子 N2的电子式误写为 ,应写为
误区 2
化合物类型不清
楚,漏写或多写[
]及错写电荷数
NaCl 误写为 ,应写为 ;
HF 误写为 ,应写为
误区 3
书写不规范,错写
共用电子对 N2的电子式误写为 或 或
误区 4
不考虑原子间的结
合顺序 HClO 的电子式误写为 ,应写为
误区 5不考虑原子最外层
有几个电子,均写 CH 的电子式误写为 ,应写为
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币





