第5章 第31讲 晶体结构与性质---2023年高考化学一轮复习(新高考)
第31 讲 晶体结构与性质
复习目标 1.了解晶体的类型,了解不同类型晶体中结构微粒、微粒间作用力的区别。2.了
解分子晶体、共价晶体、离子晶体、金属晶体结构与性质的关系。3.了解晶胞的概念,能根
据晶胞确定晶体的组成并进行相关的计算。
考点一 晶体与晶胞
1.晶体与非晶体
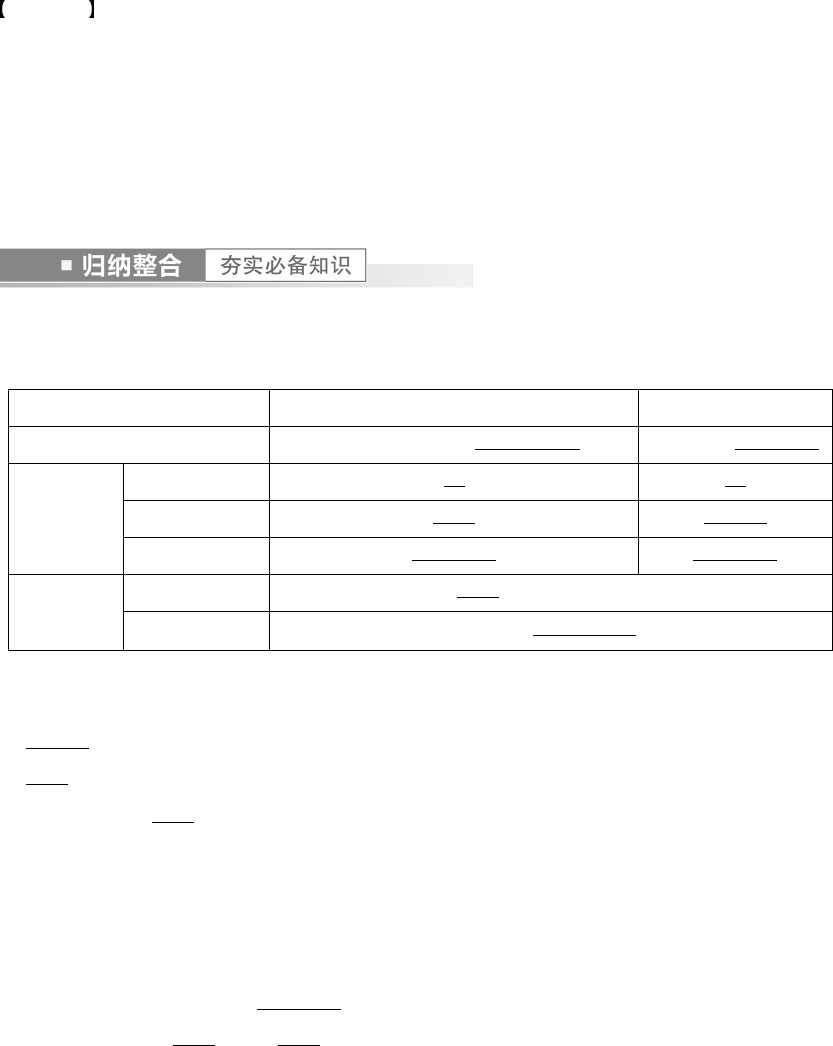
(1)晶体与非晶体的比较
晶体 非晶体
结构特征 原子在三维空间里呈周期性有序排列 原子排列相对无序
性质特征
自范性 有 无
熔点 固定 不固定
异同表现 各向异性 各向同性
二者区别
方法
间接方法 看是否有固定的熔点或根据某些物理性质的各向异性
科学方法 对固体进行 X
射线衍射 实验
(2)获得晶体的途径
① 熔融态物质凝固。
② 气态物质冷却不经液态直接凝固(凝华)。
③ 溶质从溶液中析出。
2.晶胞
(1)概念:晶胞是描述晶体结构的基本单元,是从晶体中“截取”出来具有代表性的最小重
复单元。
(2)晶体中晶胞的排列——无隙并置
① 无隙:相邻晶胞之间没有任何间隙。
② 并置:所有晶胞平行排列、取向相同。
(3)晶胞中微粒数的计算方法——均摊法
① 长方体(包括立方体)晶胞中不同位置的粒子数的计算:如某个粒子为 N个晶胞所共有,则
该粒子有属于这个晶胞。中学中常见的晶胞为立方晶胞,立方晶胞中微粒数的计算方法如图
1。

② 非长方体晶胞
在六棱柱(如图 2)中,顶角上的原子有属于此晶胞,面上的原子有属于此晶胞,因此六棱柱
中镁原子个数为 12×+2×=3,硼原子个数为 6。
1.冰和碘晶体中相互作用力相同( )
2.晶体内部的微粒按一定规律周期性排列( )
3.凡有规则外形的固体一定是晶体( )
4.固体 SiO2一定是晶体( )
5.缺角的 NaCl 晶体在饱和 NaCl 溶液中会慢慢变为完美的立方体块( )
6.晶胞是晶体中最小的“平行六面体”( )
7.区分晶体和非晶体最可靠的方法是对固体进行 X射线衍射实验( )
答案 1.× 2.√ 3.× 4.× 5.√ 6.× 7.√
一、晶胞及微粒配位数的判断
1.CaTiO3的晶胞如图所示,其组成元素的电负性大小顺序是__________;金属离子与氧离
子间的作用力为______________,Ca2+的配位数是__________。
答案 O>Ti>Ca 离子键 12
2.C、N元素能形成一种类石墨的聚合物半导体 g-C3N4,其单层平面结构如图 1,晶胞结构
如图 2。
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币





