第6章 第33讲 反应热---2023年高考化学一轮复习(新高考)

第33 讲 反应热
复习目标 1.了解反应热、焓变的概念,知道化学反应热效应与反应的焓变之间的关系。
2.知道常见的吸热反应和放热反应,能从多角度分析化学反应中能量变化的原因。 3.了解热
化学方程式的含义,能正确书写热化学方程式。
考点一 反应热 焓变
1.反应热和焓变
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境吸收的热量。
(2)焓变
① 焓(H):焓是与内能有关的物理量。
② 焓变(ΔH):生成物的焓与反应物的焓之差。
③ 焓变与反应热的关系
等压条件下的反应热等于反应的焓变,常用 Δ H
表示反应热,常用单位:kJ·mol -
1
。
2.吸热反应、放热反应
(1)放热反应:释放热量的化学反应。反应物的总能量大于生成物的总能量。反应体系的能
量降低,故 ΔH<0,即 ΔH为负值。
(2)吸热反应:吸收热量的化学反应。反应物的总能量小于生成物的总能量。反应体系的能
量升高,故 ΔH>0,即 ΔH为正值。
(3)常见的吸热反应和放热反应
吸热反应(ΔH>0) 放热反应(ΔH<0)
①Ba(OH)2·8H2O与NH4Cl 的反应
② 大多数的分解反应
③ 弱电解质的电离
④ 盐类水解
⑤C和H2O(g)、C和CO2的反应
① 中和反应
② 燃烧反应
③ 金属与酸或氧气的反应
④ 铝热反应
⑤ 酸性氧化物或碱性氧化
物与水的反应
⑥ 大多数的化合反应
3.反应热产生的原因
1.浓H2SO4稀释是放热反应( )
2.放热反应不需要加热就能反应,吸热反应不加热就不能反应( )
3.可逆反应的 ΔH表示完全反应时的热量变化,与反应是否可逆无关( )
4.吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量 (
)
5.活化能越大,表明化学反应吸收的能量越大( )
答案 1.× 2.× 3.√ 4.√ 5.×
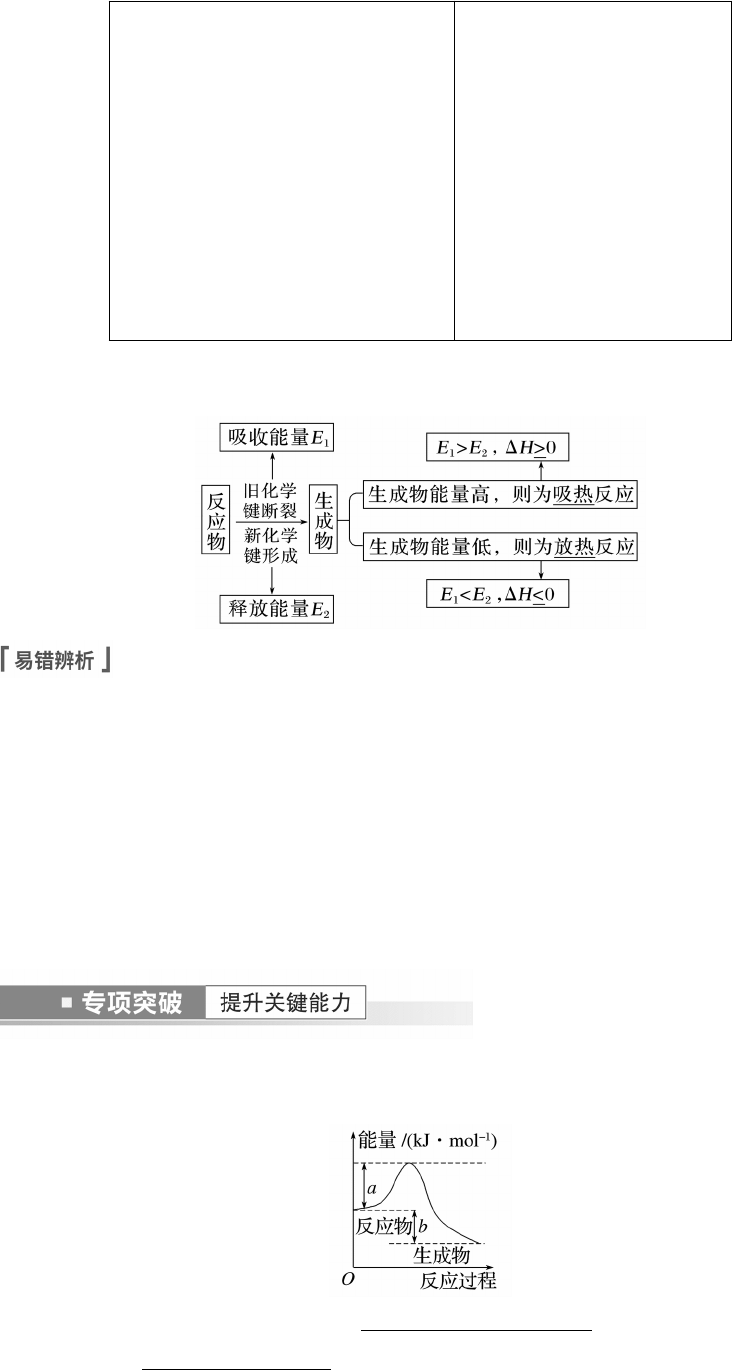
一、理解反应热与物质的能量变化关系图
1.根据如图所示的反应,回答下列问题:
(1)该反应是放热反应,还是吸热反应? 。
(2)反应的 ΔH= 。
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币





