(2)比较金属的活动性强弱:原电池中,负极一般是活动性较强的金属,正极一般是活动性
较弱的金属(或能导电的非金属)。
(3)加快化学反应速率:氧化还原反应形成原电池时,反应速率加快。
(4)用于金属的防护:将需要保护的金属制品作原电池的正极而受到保护。
1.理论上,任何自发的氧化还原反应都可设计成原电池( )
2.放热反应都可设计成原电池( )
3.在锌铜原电池中,因为有电子通过电解质溶液形成闭合回路,所以有电流产生( )
4.两种活动性不同的金属组成原电池的两极,活泼金属一定作负极( )
5.一般来说,带有“盐桥”的原电池比不带“盐桥”的原电池效率高( )
6.实验室制备 H2时,用粗锌(含Cu、Fe 等)代替纯锌与盐酸反应效果更佳( )
答案 1.√ 2.× 3.× 4.× 5.√ 6.√
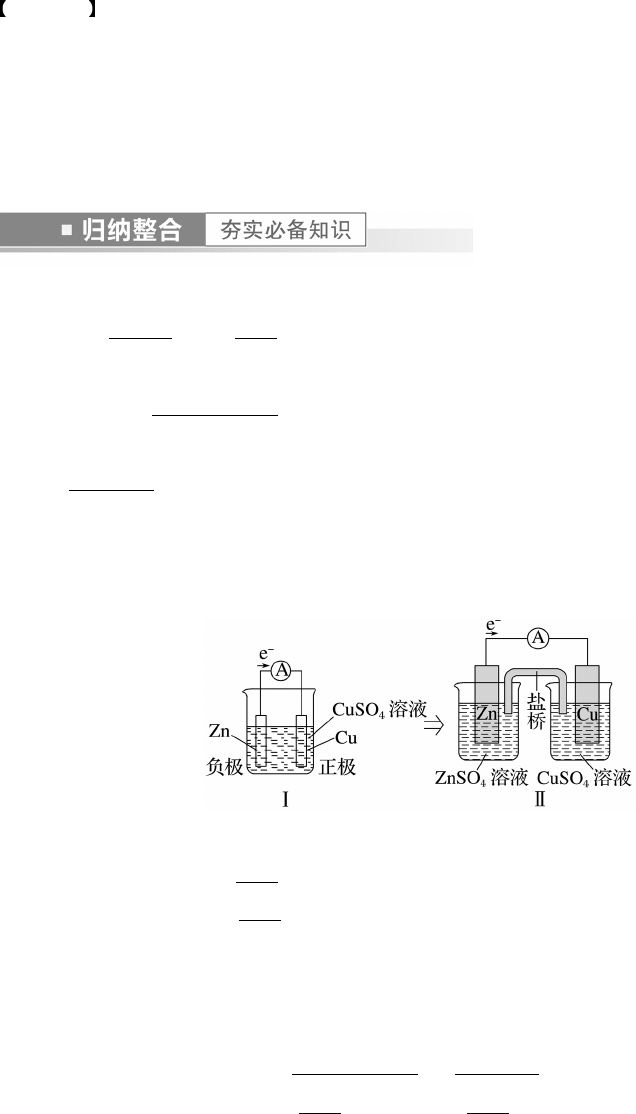
一、原电池原理及电极的判断
1.银锌电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O===Zn(OH)2+2Ag,其工
作示意图如图。下列说法不正确的是( )
A.Zn 电极发生氧化反应
B.Ag2O电极是电源的正极
C.电池工作时,电子从 Zn 电极经导线流向 Ag2O电极,再由 Ag2O电极经电解质溶液流向
Zn 电极