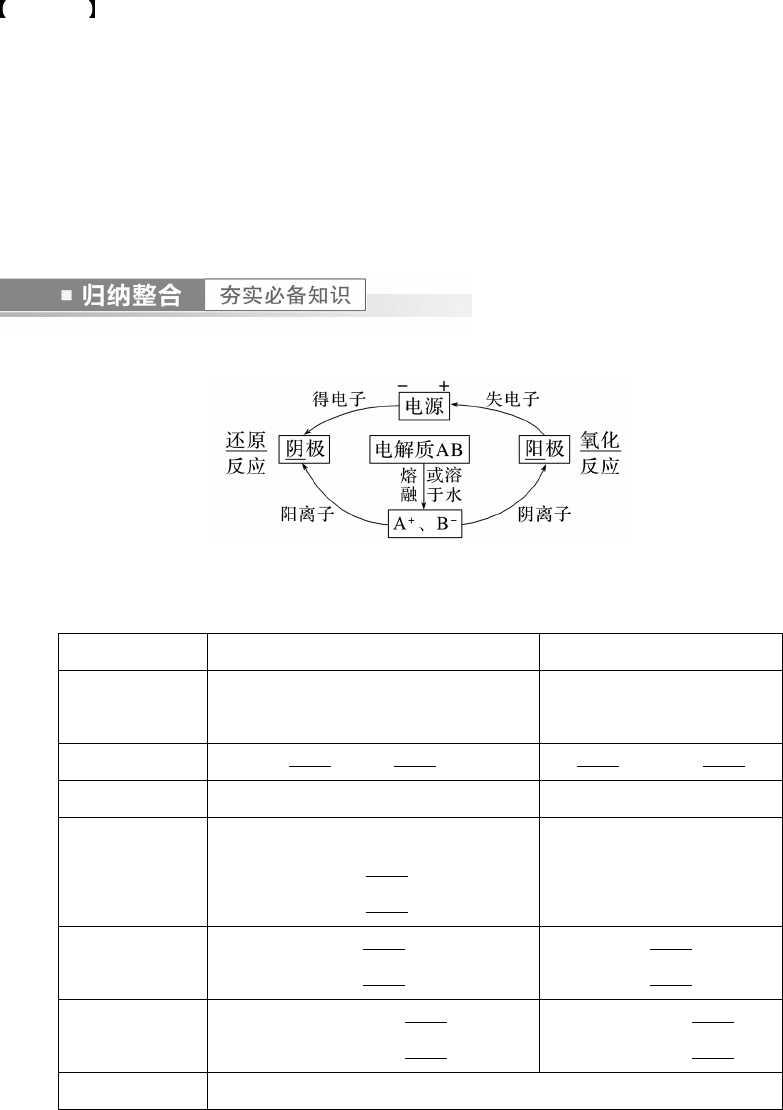
3.电解规律
(1)阳极产物的判断
① 活性电极(除Au、Pt 以外的金属材料作电极),电极材料失电子,生成金属阳离子。
② 惰性电极(Pt、Au、石墨),要依据阴离子的放电顺序加以判断。
阴离子的放电顺序:活泼电极>S2->I->Br->Cl->OH->含氧酸根离子。
S2-、I-、Br-、Cl-放电,产物分别是 S、I2、Br2、Cl2;若 OH-放电,则得到 H2O和O2。
(2)阴极产物的判断
直接根据阳离子放电顺序进行判断。
阳离子放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+。
① 若金属阳离子(Fe3+除外)放电,则得到相应金属单质;若 H+放电,则得到 H2。
② 放电顺序本质遵循氧化还原反应的优先规律,即得(失)电子能力强的离子先放电。
1.电解 CuCl2溶液,阴极逸出的气体能够使湿润的淀粉碘化钾试纸变蓝色( )
2.电解质溶液的导电过程就是电解质溶液被电解的过程( )
3.电解盐酸、硫酸溶液等,H+放电,溶液的 pH 逐渐增大( )
4.用 Cu 作电极电解盐酸可发生 Cu+2H+=====Cu2++H2↑( )
5.某些不能自发进行的氧化还原反应,通过电解可以实现( )
6.电解过程中电子流动方向为负极→阴极→电解质溶液→阳极→正极( )
答案 1.× 2.√ 3.× 4.√ 5.√ 6.×
1.完成下表(电极为惰性电极)
类型 实例 电极反应式 电解
对象
溶液
pH 变化
溶液复原
方法
电解
水型
含氧酸 H2SO4
阳极:2H2O-4e-===4H++O2↑
阴极:4H++4e-===2H2↑
总反应:2H2O=====2H2↑+O2↑
水
减小
加水强碱 NaOH
阳极:4OH--4e-===2H2O+O2↑
阴极:4H2O+4e-===2H2↑+4OH-
总反应:2H2O=====2H2↑+O2↑
增大
活泼金属
的含氧酸
盐
KNO3
阳极:2H2O-4e-===4H++O2↑
阴极:4H2O+4e-===2H2↑+4OH-
总反应:2H2O=====2H2↑+O2↑
不变
电解电
解质型
无氧酸
(氢氟酸
除外)
HCl
阳极:2Cl--2e-===Cl2↑
阴极:2H++2e-===H2↑
总反应:2H++2Cl-=====H2↑+Cl2↑
HCl 增大 通入