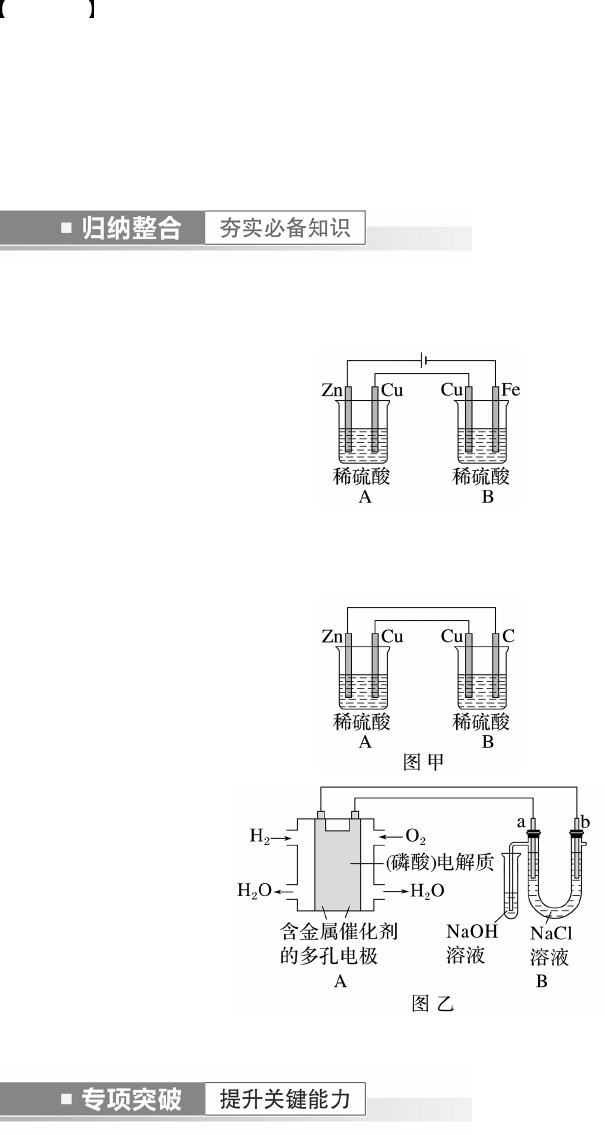
请回答下列问题:
(1)甲池为________(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应
式为________________________________________________________________________
________________________________________________________________________。
(2)乙池中 A(石墨)电极的名称为________(填“正极”“负极”“阴极”或“阳极”),总反
应式为________________________________________________________________________
________________________________________________________________________。
(3)当乙池中 B极质量增加 5.40 g 时,甲池中理论上消耗 O2的体积为________mL(标准状况
下),丙池中________极析出________g 铜。
(4)若丙池中电极不变,将其溶液换成 NaCl 溶液,电键闭合一段时间后,甲池中溶液的 pH
将______(填“增大”“减小”或“不变”,下同);丙池中溶液的 pH 将________。
答案 (1)原电池 CH3OH-6e-+8OH-===CO+6H2O (2)阳极 4AgNO3+2H2O=====4Ag
+O2↑+4HNO3 (3)280 D 1.60 (4)减小 增大
解析 (1)甲池为原电池,通入 CH3OH 的电极为负极,电极反应式为 CH3OH-6e-+8OH-
===CO+6H2O。
(2) 乙池中电解 AgNO3溶液,其中 C作阳极,Ag 作阴极,总反应式为 4AgNO3+
2H2O=====4Ag+O2↑+4HNO3。
(3)根据各电极上转移的电子数相同,得 n(Ag)=4n(O2)=2n(Cu),故 V(O2)=××22.4 L=0.28
L=280 mL,m(Cu)=××64 g=1.60 g。(4)若丙池中电极不变,将其溶液换成 NaCl 溶液,根
据丙池中总反应 2NaCl+2H2O=====2NaOH+H2↑+Cl2↑,则溶液 pH 增大,而甲池中
总反应为 2CH3OH+3O2+4KOH===2K2CO3+6H2O,溶液 pH 减小。
2.中科院长春应化所张新波团队提出了一种独特的锂—氮电池(Li—N2),该电池在放电过
程中消耗氮气,充电过程中释放氮气,实现氮气的循环,并对外提供电能。该电池在充电时
发生反应:2Li3N===N2↑+6Li。现以该电池为电源进行如图所示实验,下列说法正确的是(
)