热点强化 12 化学反应历程、机理的分析应用
1.大多数的化学反应不能一步完成,在微观上是分几步完成的,每一步反应都叫一个基元
反应。
如反应:H2O2+2Br-+2H+===Br2+2H2O,通过大量实验提出它们微观过程如下:
(1)H++H2O2H3O;
(2)H3O+Br-===H2O+HOBr;
(3)HOBr+H++Br-===H2O+Br2。
2.基元反应过渡状态理论
基元反应过渡状态理论认为,基元反应在从反应物到生成物的变化过程中要经历一个中间状
态,这个状态称为过渡态。
AB+C―→[A…B…C]―→A+BC
反应物 过渡态 生成物
过渡态是处在反应过程中具有最高能量的一种分子构型,过渡态能量与反应物的平均能量的
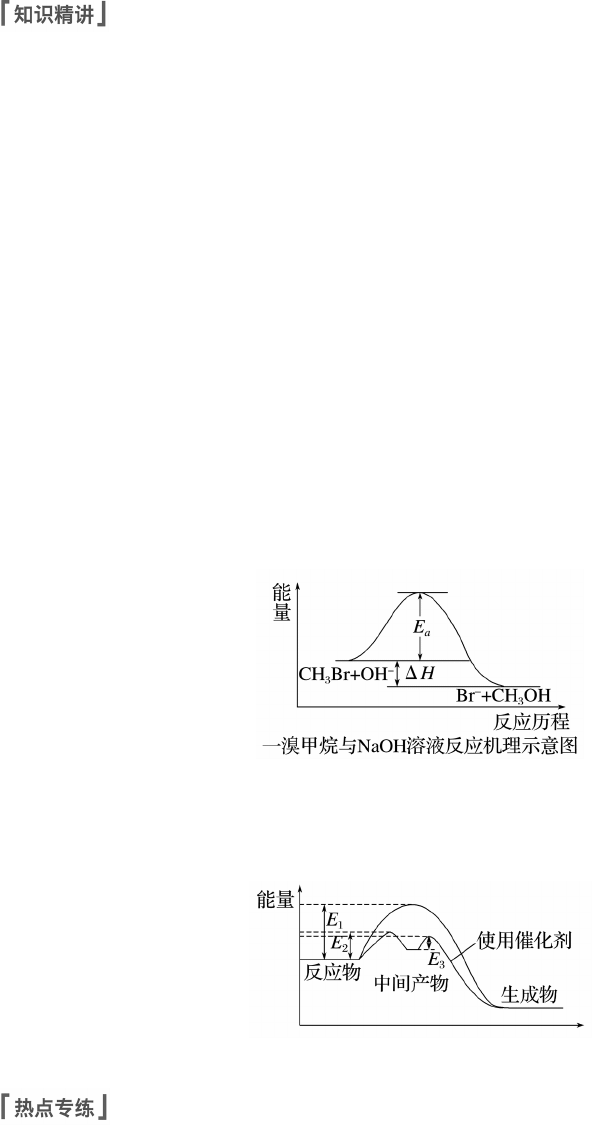
差值相当于活化能[活化能(能垒)越高,此步基元反应速率越慢]。例如,一溴甲烷与 NaOH
溶液反应的过程可以表示为 CH3Br+OH-―→[Br…CH3…OH]―→Br-+CH3OH
3.活化能与反应机理
使用催化剂,可以改变活化能,改变反应机理,在反应机理中每一步反应的活化能不同,且
均比总反应的活化能低,故一般使用催化剂可以降低反应活化能,加快反应速率,如图所示:
E1为总反应的活化能,E2、E3为使用催化剂反应机理中各步的活化能。
1.已知反应 2NO(g)+2H2(g)N2(g)+2H2O(g)
ΔH=-752 kJ·mol-1的反应机理如下: