专项特训 7 化工流程中的 Ksp 计算
1.[2021·广东,18(1)(2)(3)]对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝
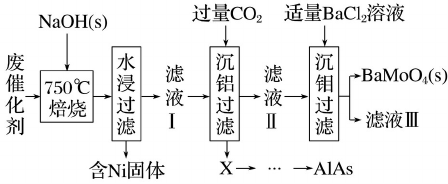
(Al)、钼(Mo)、镍(Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25 ℃时,H2CO3的Kal =4.5×10-7,Ka2 =4.7×10-11 ;Ksp( BaMoO4)=3.5×10-8;
Ksp(BaCO3)=2.6×10-9;该工艺中,pH>6.0 时,溶液中 Mo 元素以 MoO 的形态存在。
(1)“焙烧”中,有 Na2MoO4生成,其中 Mo 元素的化合价为__________。
(2)“沉铝”中,生成的沉淀 X为________。
(3)“沉钼”中,pH 为7.0。
① 生成 BaMoO4的离子方程式为___________________________________________
________________________________________________________________________。
② 若 条 件 控 制 不当 , BaCO3也 会 沉 淀 。 为 避 免 BaMoO4中 混 入 BaCO3沉 淀 , 溶液 中
c(HCO)∶c(MoO)=______________________________(列出算式)时,应停止加入 BaCl2溶液。
答案 (1)+6 (2)Al(OH)3 (3)①MoO+Ba2+===BaMoO4↓ ②
解析 (1)“焙烧”中,有 Na2MoO4生成,其中 Na 和O的化合价分别为+1和-2,根据化
合物中各元素化合价的代数和为 0可知,Mo 元素的化合价为+6。
(2)“沉铝”中,偏铝酸钠转化为氢氧化铝,因此,生成的沉淀 X为Al(OH)3。
(3)①滤液Ⅱ中含有钼酸钠,加入氯化钡溶液后生成 BaMoO4沉淀,该反应的离子方程式为
MoO+Ba2+===BaMoO4↓。②若开始生成 BaCO3沉淀,则体系中恰好建立如下平衡:HCO
+BaMoO4BaCO3+MoO+H+,该反应的化学平衡常数 K===。为避免 BaMoO4中混入
BaCO3沉淀,必须满足≤,由于“沉钼”中pH 为7.0,c(H+)=1×10-7 mol·
L-1,所以溶液中=时,开始生成 BaCO3沉淀, 因此,c(HCO)∶c(MoO)==时,应停止加
入BaCl2溶液。
2.Li4Ti5O12 和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿 (主要成分为 FeTiO3,还
含有少量 MgO、SiO2等杂质)来制备,工艺流程如下: