a→________、________→________、________→________、________→h(填装置口小写字
母)。
(3)该小组同学按上述顺序连接各装置并进行实验,请为他们补全表格:
装置编号 填装试剂 实验现象 实验结论
A FeSO4·7H2O绿色固体逐渐变为红色粉末 —
B①________ ②________ 分解产物中含有 SO2
CBaCl2溶液 产生白色沉淀 ③________
D无水 CuSO4粉末 白色固体逐渐变为蓝色 分解产物中含有水蒸气
E④________ — —
(4)硫酸亚铁晶体分解的化学方程式为___________________________________________
___________________________________________________________________________。
(5)设计实验证明 A中得到的红色粉末不含+2价铁元素:_________________________
_________________________________________________________(简述实验操作及现象)。
答案 (1)防止固体粉末堵塞导管 (球形)干燥管
(2)f g e d c b
(3)① 品红溶液 ②溶液由红色褪为无色 ③分解产物中含有 SO3 ④ NaOH 溶液
(4)2FeSO4·7H2O=====Fe2O3+SO2↑+SO3↑+14H2O↑
(5)取实验后反应管中的少量固体,溶于稀盐酸后,向溶液中滴加 K3[Fe(CN)6]溶液,不产生
蓝色沉淀
解析 (2)由实验目的和原理知,A中发生 FeSO4·7H2O的分解,装置 D用于检验水蒸气,装
置C用于检验 SO3,装置 B用于检验 SO2,装置 E用于尾气处理,按气流方向,装置合理的
连接顺序为 afgedcbh。(3)装置 B用于检验 SO2,可以用品红溶液褪色证明分解产物中含有
SO2;装置 C中BaCl2溶液产生白色沉淀可以证明分解产物中含有 SO3;装置 E为尾气处理,
应填装的试剂为 NaOH 溶液。
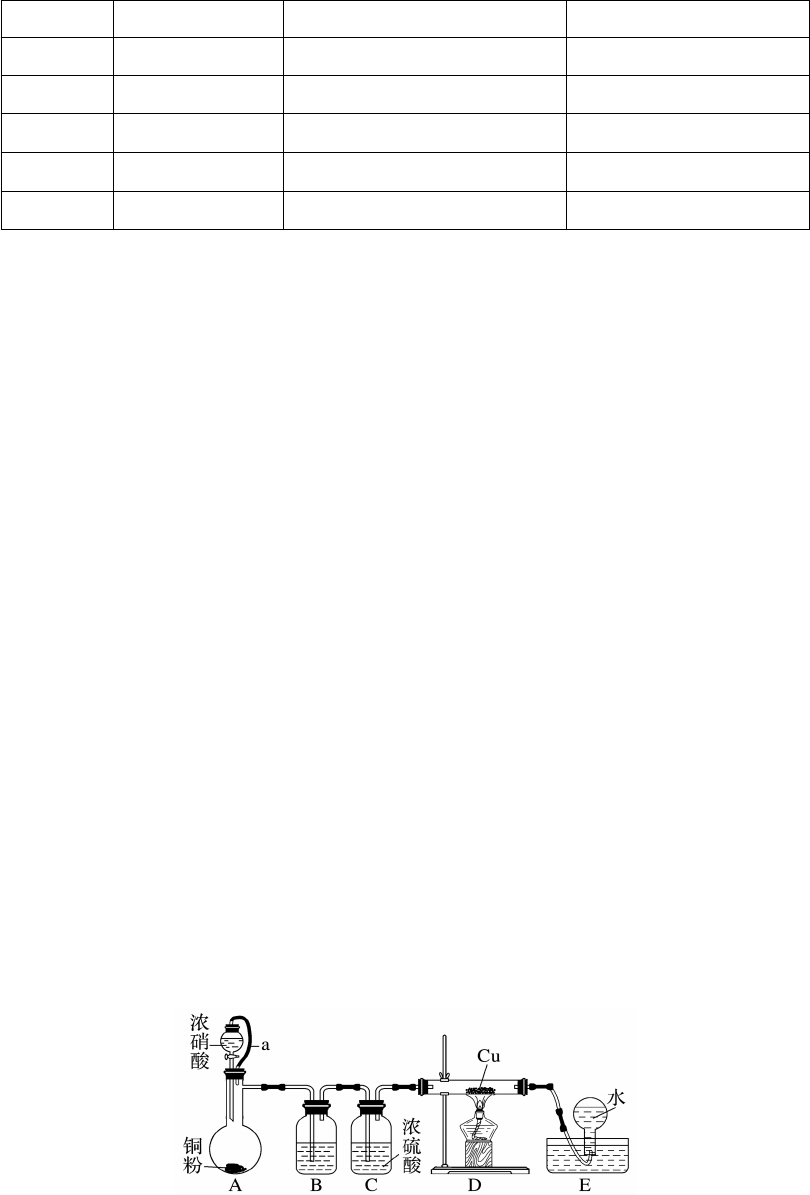
2.(2022·安庆市高三模拟)已知:① Cu2O在酸性条件下能迅速发生反应:Cu2O+2H+===Cu
+Cu2++H2O;②氮的氧化物能与红热的铜反应。某小组设计实验探究 NO 和Cu 反应的氧
化产物,装置如图所示(部分夹持装置未画出)。
请回答下列问题: