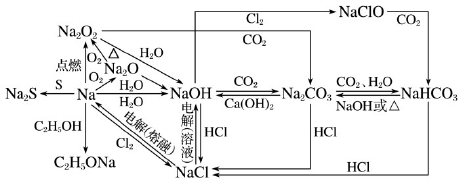
题组一 重要反应规范书写
1.用方程式回答下列问题
(1)实验室怎样处理钠屑?
__________________________________________________
(2)写出 Na 与CuSO4溶液反应的离子方程式。
__________________________________________________
(3)怎样将 Na2CO3溶液转化为 NaOH 溶液(用化学方程式表示)。
__________________________________________________
(4)向NaOH、Na2CO3、NaHCO3溶液中逐滴加入盐酸,发生反应的离子方程式。
__________________________________________________
(5)怎样除去 CO2中的 SO2气体(用离子方程式表示)。
__________________________________________________
(6)怎样除去 Na2CO3溶液中的 NaHCO3(用离子方程式表示)。
__________________________________________________
(7)怎样除去 NaHCO3溶液中的 Na2CO3(用离子方程式表示)。
__________________________________________________
(8)用化学方程式表示呼吸面具中产生 O2的原理。
__________________________________________________
题组二 高考选择强化练习
2.正误判断,正确的划“√”,错误的划“×”。
(1)钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火( )
(2)灼烧白色粉末,火焰呈黄色,证明原粉末中有 Na+,无 K+( )
(3)钠在空气中燃烧可生成多种氧化物。23 g 钠充分燃烧时转移电子数为 NA( )
(4)将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡( )
(5)过氧化钠与水反应时,生成 0.1 mol 氧气转移的电子数为 0.2NA( )
(6)分别加热 Na2CO3和NaHCO3固体,试管内壁均有水珠,则两种物质均受热分解( )
(7)用热的烧碱溶液洗去油污,是因为 Na2CO3可直接与油污反应( )
(8)用热碱水清除炊具上残留的油污发生了化学变化( )
(9)二氧化碳通过 Na2O2粉末反应后固体物质增重( )
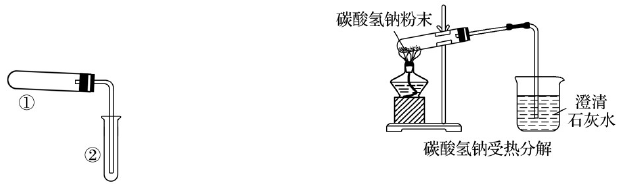
(10)①中为 NaHCO3固体受热分解,②中为澄清石灰水变
浑浊,由②中现象,能证实①中发生的反应( )
(11)除去 Na2CO3固体中的 NaHCO3固体可用灼烧的方法( )
考点二 铝及其重要化合物