(1)观察法:氯气是黄绿色气体
(2)将湿润的淀粉碘化钾试纸靠近盛氯气的瓶口,观察到试纸立即变蓝,则证明已集满
(3)将湿润的蓝色石蕊试纸靠近盛氯气的瓶口,观察到试纸立即发生先变红后褪色的变化,则证明已集满
【微点拨】
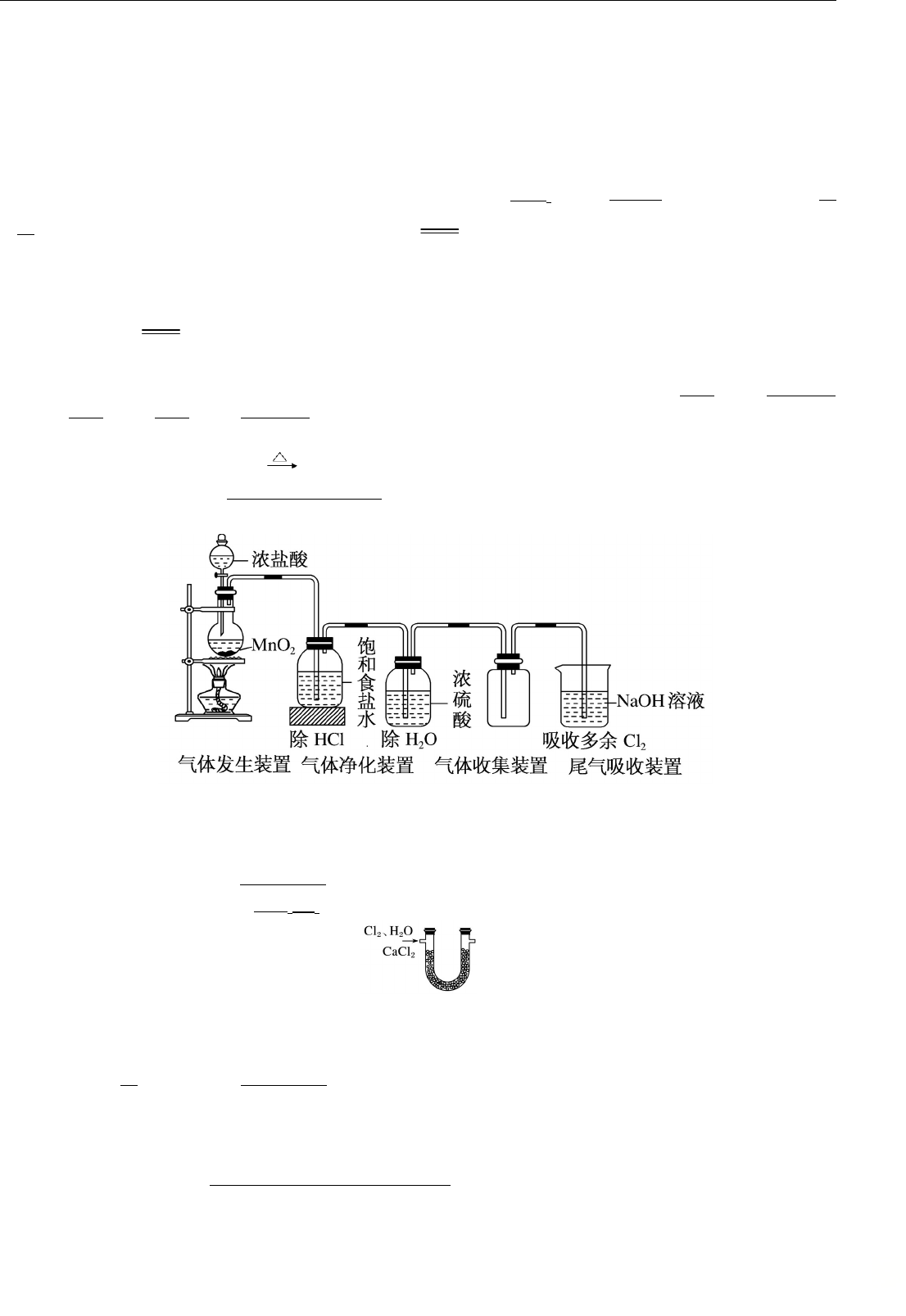
① 必须用浓盐酸,MnO2与稀盐酸不反应,且随着反应的进行,盐酸浓度变小,无论 MnO2是否足量,盐酸均
不能完全反应,反应后的溶液为盐酸和 MnCl2的混合液
② 浓盐酸中,部分 Cl-的化合价升高,4 mol HCl 参加反应,被氧化的 Cl-为2 mol
③ 为了减少制得的 Cl2中HCl 的含量,加热温度不宜过高,减少 HCl 的挥发
④Cl2有毒,必须有尾气吸收装置,常用吸收剂为 NaOH 溶液或碱石灰,不用澄清石灰水,因澄清石灰水中
Ca(OH)2浓度小,吸收慢且吸收不完全
⑤ 实验结束后,先使反应停止并排出装置中残留的 Cl2,再拆卸装置,避免污染空气
【即学即练 1】
1、将 0.2 mol MnO2和50 mL 12 mol·L-1的盐酸混合后缓缓加热,向反应完全后的溶液中加入足量 AgNO3溶液,
则生成的 AgCl 沉淀的物质的量(不考虑盐酸的挥发)( )
A.等于 0.3 mol B.小于 0.3 mol
C.在0.3~0.6 mol 之间 D.以上结论均不正确
2、实验室用下列两种方法制氯气:①用含 HCl 146 g 的浓盐酸与足量的 MnO2反应;②用 87 g MnO2与足量浓盐
酸反应。所得的氯气( )
A.①比②多 B.②比①多 C.一样多 D.无法比较
3、实验室用 MnO2和浓盐酸制取氯气时,有 14.6 g 氯化氢被氧化,所得 Cl2全部用石灰水吸收,可制得漂白粉
的质量是( )
A.14.3 g B.25.4 g C.28.6 g D.50.8 g
4、某化学兴趣小组利用MnO2和浓盐酸及如图装置制备Cl2。下列分析中不正确的是( )
A.①中可用分液漏斗代替长颈漏斗 B.①中缺少加热装置
C.②中盛放的NaOH 溶液可以净化氯气 D.④中盛放的NaOH 溶液可以吸收尾气
5、下列关于实验室制取 Cl2的说法正确的是( )
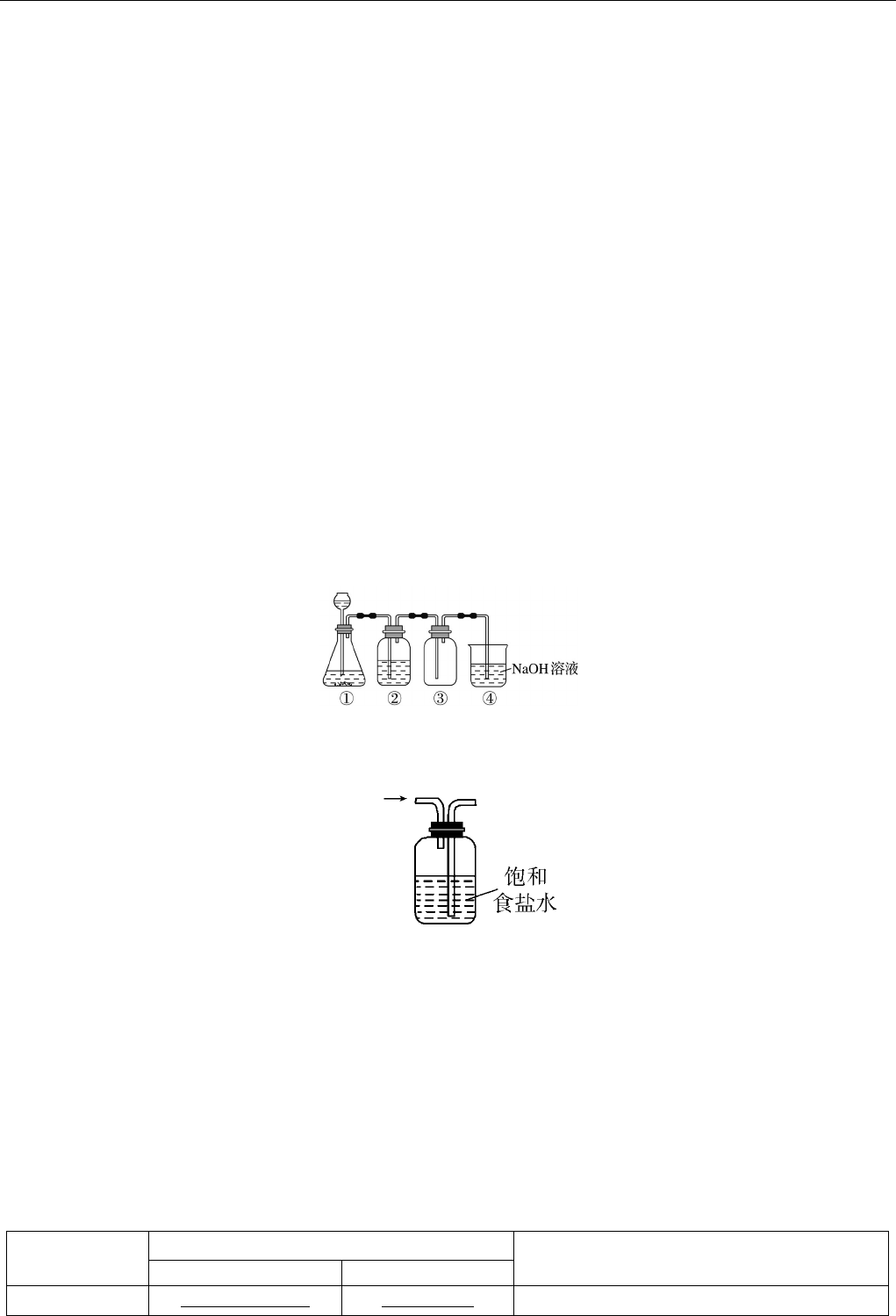
A.将混有 HCl 杂质的 Cl2通过盛有饱和 NaHCO3溶液的洗气瓶除去杂质
B.实验室制取 Cl2,浓盐酸起到酸性和氧化剂作用
C.实验室用如图装置除去 Cl2中的少量 HCl
D.实验室制备Cl2,可用排饱和食盐水集气法收集
6、检验Cl2是否充满了集气瓶的正确操作为( )
A.用玻璃棒粘上湿润的淀粉KI 试纸伸到集气瓶口附近,观察试纸是否变蓝
B.将AgNO3溶液滴入集气瓶中,观察有无白色沉淀生成
C.用玻璃棒蘸取少许NaOH 溶液放入集气瓶口附近,看是否反应
D.用手将湿润的淀粉KI 试纸放在集气瓶口上方,观察颜色是否变蓝
二、氯离子的检验
【思考与交流】在3支试管中分别加入2~3 mL 稀盐酸、NaCl 溶液、Na2CO3溶液,然后各滴入几滴 AgNO3溶
液,观察现象。再分别加入少量稀硝酸,观察现象
实验现象 解释或相关化学方程式
滴入几滴 AgNO3溶液 再加入少量稀硝酸
①稀盐酸 有白色沉淀生成 沉淀不溶解 HCl+AgNO3===AgCl↓+HNO3