专题18 物质结构与性质(选修)——2020-2022年高考化学真题分项汇编(新高考专用)(解析版)
专题 18 物质结构与性质(选修)
1.(2022·广东卷)硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我
国科学家发现聚集诱导发光( )效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
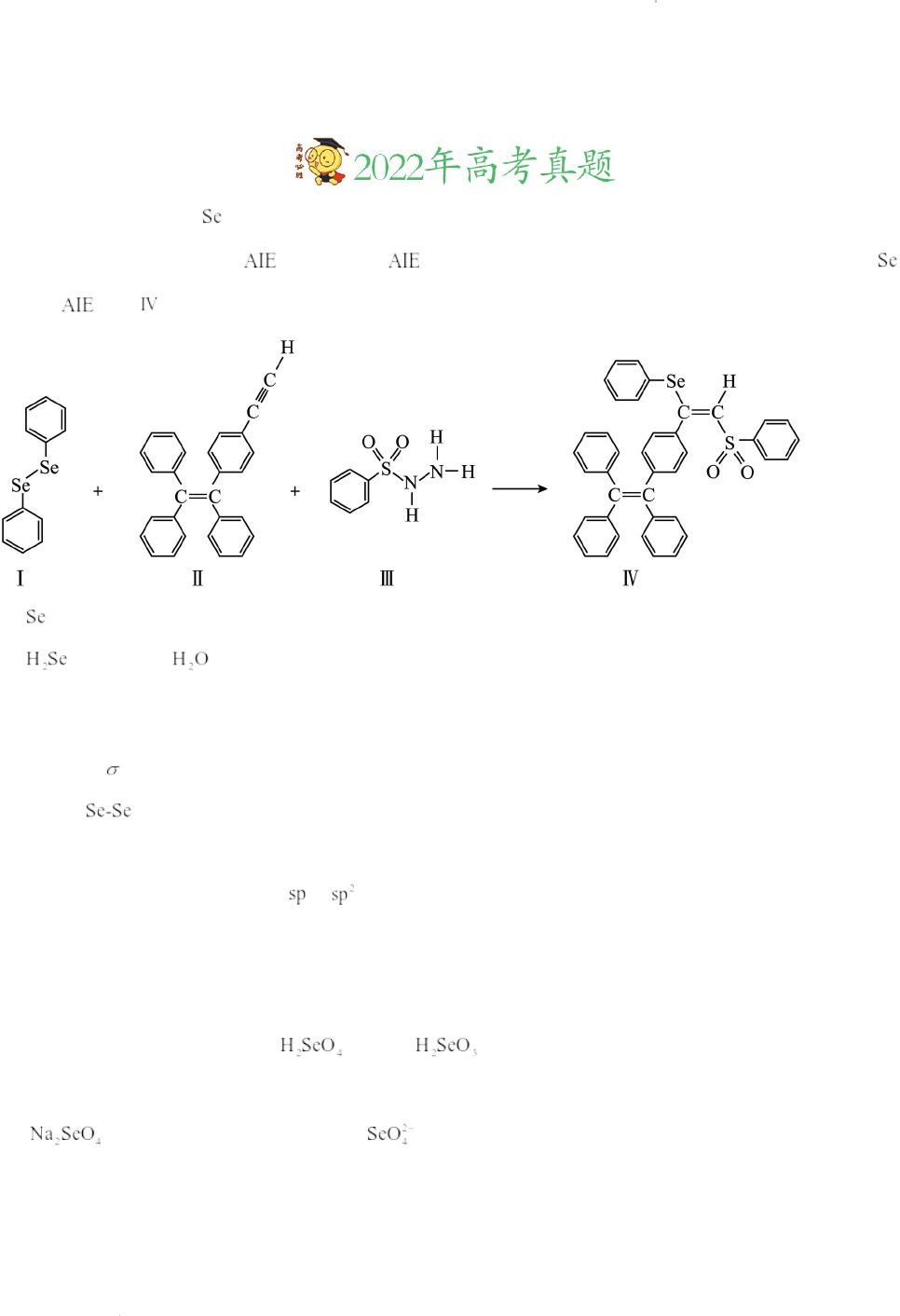
的新型 分子 的合成路线如下:
(1) 与S同族,基态硒原子价电子排布式为_______。
(2) 的沸点低于 ,其原因是_______。
(3)关于 I~III 三种反应物,下列说法正确的有_______。
A.I中仅有 键
B.I中的 键为非极性共价键
C.II 易溶于水
D.II 中原子的杂化轨道类型只有 与
E.I~III 含有的元素中,O电负性最大
(4)IV 中具有孤对电子的原子有_______。
(5)硒的两种含氧酸的酸性强弱为 _______ (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸
钠( )可减轻重金属铊引起的中毒。 的立体构型为_______。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速
新型热电材料的研发进程。化合物 X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图 1,沿
x、y、z轴方向的投影均为图 2。
学科网(北京)股份有限公司

①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则 X中相邻 K之间的最短距离为_______ (列出计
算式, 为阿伏加德罗常数的值)。
【答案】(1)4s24p4
(2)两者都是分子晶体,由于水存在分子间氢键,沸点高
(3)BDE
(4)O、Se
(5)>ÜÜÜÜ 正四面体形
(6) K2SeBr6
【解析】(1)基态硫原子价电子排布式为 3s23p4, 与 S同族,Se 为第四周期元素,因此基态硒原子价电子
排布式为 4s24p4。
(2) 的沸点低于 ,其原因是两者都是分子晶体,由于水存在分子间氢键,沸点高。
(3)A.I中有 键,还有大 π键,故 A错误;B.Se−Se 是同种元素,因此 I中的 键为非极性共价键,
故B正确;C.烃都是难溶于水,因此 II 难溶于水,故 B错误;D.II 中苯环上的碳原子和碳碳双键上的
碳原子杂化类型为 sp2,碳碳三键上的碳原子杂化类型为 sp,故 D正确;E.根据同周期从左到右电负性逐
渐增大,同主族从上到下电负性逐渐减小,因此 I~III 含有的元素中,O电负性最大,故 E正确;综上所述,
答案为:BDE。
(4)根据题中信息 IV 中O、Se 都有孤对电子,碳、氢、硫都没有孤对电子。
(5)根据非羟基氧越多,酸性越强,因此硒的两种含氧酸的酸性强弱为 > 。 中 Se 价层
学科网(北京)股份有限公司
免费试读已结束,如果需要继续阅读,请您下载
本文档需要3知币

