6. NA代表阿伏加德罗常数的值。下列说法正确的是
A.2.2g 超重水(3H2O)所含的电子数目为 NA
B.1L 0.1mol·L-1 NaClO 溶液中 ClO-的数目为 0.1NA
C.过量 C与1mol SiO2充分反应转移电子数目为 3NA
D.1mol Cl2与足量 CH4发生取代反应生成 HCl 分子的数目为 2NA
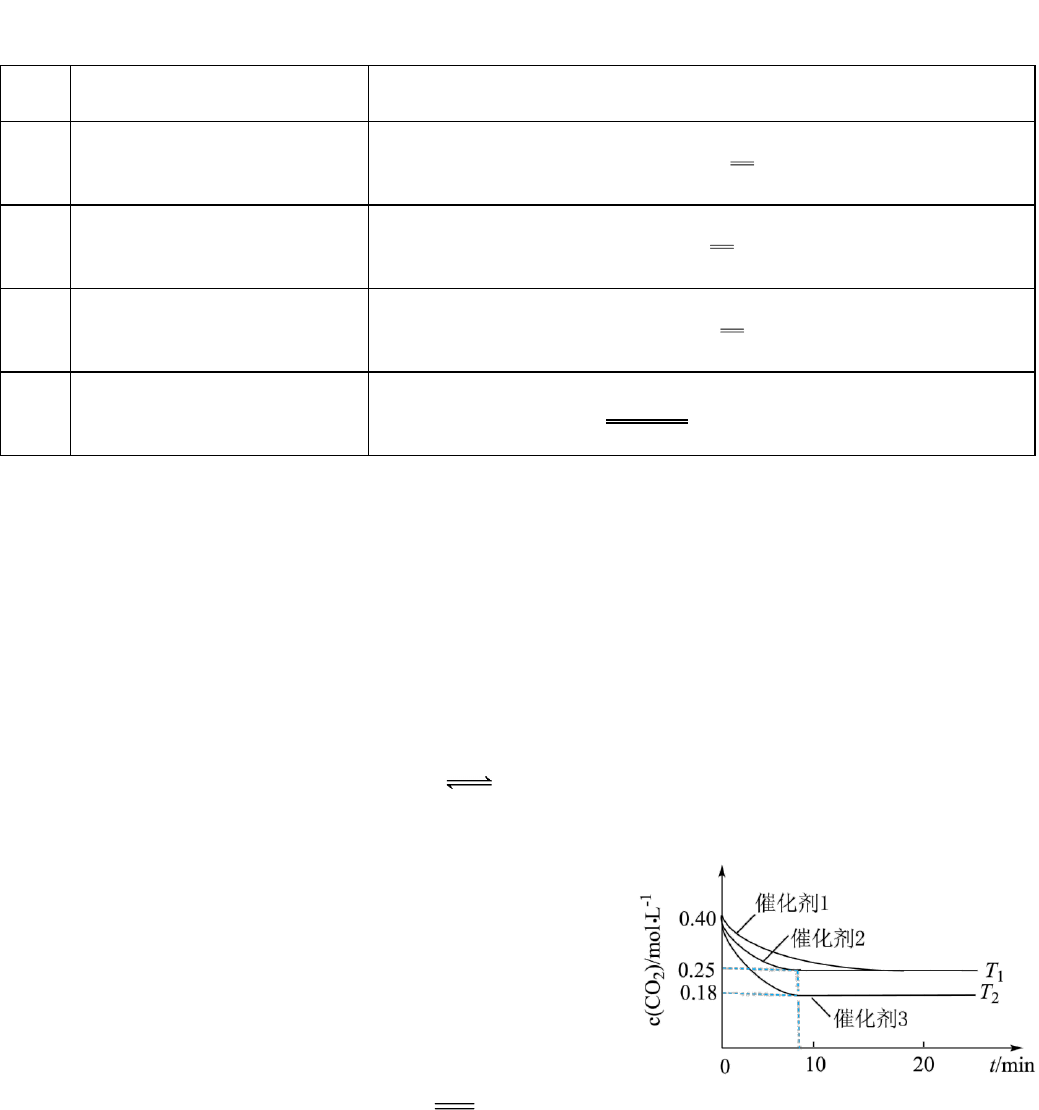
7. 已知 298K,101kPa 时,CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H=-49.5kJ ∙ mol-1。该反应在密
闭的刚性容器中分别于 T1、T2温度下进行,CO2的初始浓度为 0.4mol·L-1,c(CO2)—t关系如图所示。
下列说法错误
..
的是
A.T1>T2
B.T1下反应达到平衡时 c(CH3OH)=0.15mol·L-1
C.使用催化剂 1的反应活化能比催化剂 2的大
D.使用催化剂 2和催化剂 3的反应历程相同
8. 已知 298K,101kPa 时,2H2(g)+O2(g) 2H2O(l) ∆H=-571.6 kJ ∙ mol-1,H2的临界温度(能够液
化的最高温度)为32.98K,下列说法错误
..
的是
A.氢气燃烧热∆H=-285.8 kJ ∙ mol-1
B.题述条件下 2mol H2和1mol O2,在燃料电池中完全反应,电功+放热量 = 571.6 kJ
C.氢能利用的关键技术在于安全储存与运输
D.不同电极材料电解水所需电压不同,产生 2g H2(g)消耗的电功相同