高三复习化学大题
1.Na2S2O4俗称保险粉,常用做纺织工业的漂白剂、脱色剂等。某科研小组制备并探究其性质。
资料:Na2S2O4易溶于水,具有极强的还原性,易被空气氧化,在碱性介质中稳定。
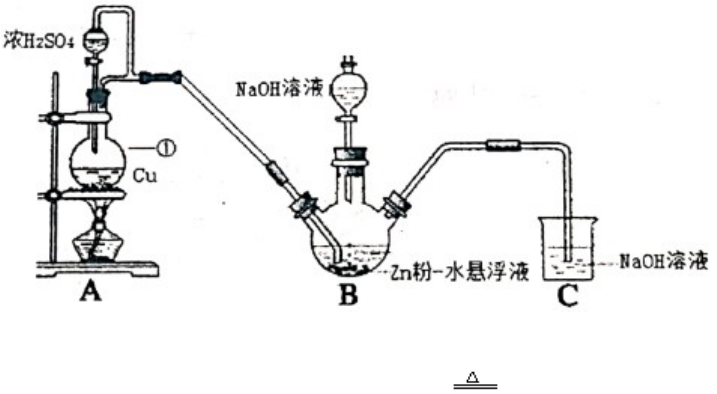
Ⅰ.制备 Na2S2O4 (部分加热等辅助仪器略去)
(1)仪器①的名称是___________。
(2)B 装置用于制备 Na2S2O4。第一步反应:Zn+2SO2ZnS2O4;第二步,加入 NaOH 溶液,于 28~35℃下反应
生成 Na2S2O4,该步反应的化学方程式为___________。
(3)实验时,先向 B 中通入 SO2的原因,除产生 Zn S2O4之外,另一原因是___________。
(4)反应后除去 B 中的沉淀,在滤液中加入一定量的 NaCl 固体搅拌,有 Na2S2O4晶体析出。加入 NaCl 固体的
作用是___________
Ⅱ.探究 Na2S2O4的性质
(5)隔绝空气加热 Na2S2O4固体完全分解得到固体产物 Na2SO3、Na2S2O3和 SO2,但科研小组没有做到完全隔绝
空气,得到的固体产物中还含有 Na2SO4。请设计实验证明该分解产物中含有 Na2SO4。实验方案是_________
__。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液、KMnO4,溶液)
(6)制备纳米级银粉用 NaOH 溶液溶解 Na2S2O4,加入一定量的 AgNO3溶液,生成纳米级的银粉。在制备银粉
的反应中,氧化剂和还原剂的物质的量之比为 2:1,且生成的含硫物质只有一种,写出该反应的离子方程
式___________。
(7)为测定某含硫代硫酸钠样品的纯度(其它杂质均不参加反应)设计如下方案,并进行实验:
① 准确称取该硫代硫酸钠样品 mg,配制成 250mL 待测溶液。
② 移取 25.00mL 待测溶液于锥形瓶中,加入少量淀粉溶液,用 nmol·L-1I2标准溶液滴定(发生反应: